题目内容
【题目】下列表示对应化学反应的离子方程式正确的是
A.在火柴头浸取的水溶液中滴入AgNO3溶液,稀硝酸溶液检验氯元素时离子反应:Ag++Cl-=AgCl↓
B.NaNO2溶液中滴加适量稀盐酸:2![]() +2H+=H2O+NO↑+NO2↑
+2H+=H2O+NO↑+NO2↑
C.向Cu(NO3)2溶液中加入过量氨水:Cu2++2NH3H2O= Cu(OH)2↓+2![]()
D.苯酚与三氯化铁溶液反应,得到溶液显紫色:6C6H5O-+Fe3+=[Fe(OC6H5)6]3-
【答案】B
【解析】
A.火柴头含有氯酸钾,浸于水中片刻后的溶液,溶液中Cl以ClO3-的形式存在,故A错误;
B.NaNO2溶液中滴加适量稀盐酸发生歧化反应生成氯化钠、NO、NO2、H2O,反应方程式是2![]() +2H+=H2O+NO↑+NO2↑,故B正确;
+2H+=H2O+NO↑+NO2↑,故B正确;
C.向Cu(NO3)2溶液中加入过量氨水生成[Cu(NH3)4]2+,故C错误;
D.苯酚是弱电解质,离子方程式中苯酚不能拆写为离子,苯酚与三氯化铁溶液反应的离子方程式是苯酚与三氯化铁溶液反应,6C6H5OH+Fe3+=[Fe(OC6H5)6]3-+ 6H+,故D错误;
选B。

 阅读快车系列答案
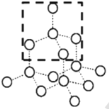
阅读快车系列答案【题目】观察下列模型并结合有关信息,判断下列说法不正确的是( )
晶体硼(其每个结构单元中有12个B原子) | NaCl | S8 | HCN | |
结构模型示意图 |
|
|
|
|
备注 | 熔点2573K | —— | 易溶于CS2 | —— |
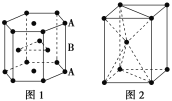
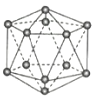
A.晶体硼属于原子晶体,结构单元中含有30个B-B键,含20个正三角形
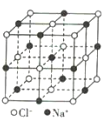
B.NaCl晶体中每个Na+周围距离最近且相等的Na+有6个
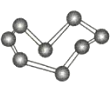
C.S8分子中的共价键为非极性键
D.HCN分子中含有2个σ键,2个π键
【题目】(I)某原料经测定主要含有A、B、C、D四种原子序数依次增大的短周期元素,其相关信息如下:
元素 | 元素性质或原子结构 |
A | 周期表中原子半径最小的元素 |
B | 原子核外有三种不同的能级且各个能级所填充的电子数相同 |
C | 最外层p轨道半充满 |
D | 位于短周期,其原子的核外成对电子数是未成对电子数的3倍 |
请回答下列问题(用A、B、C、D、所对应的元素符号作答):
(1) B、C、D第一电离能由大到小的顺序为__________________________________
(2)![]() 常用作除锈剂,该分子中B的杂化方式为_____;1 mol
常用作除锈剂,该分子中B的杂化方式为_____;1 mol ![]() 分子中含有σ键与π键的数目之比为_____。
分子中含有σ键与π键的数目之比为_____。
(3) ![]() 分子中均含有18个电子,它们的沸点相差较大,主要原因是_____________________
分子中均含有18个电子,它们的沸点相差较大,主要原因是_____________________
(Ⅱ)化学与生活密切相关。K2Cr2O7曾用于检测司机是否酒后驾驶:Cr2O![]() (橙色)+CH3CH2OH
(橙色)+CH3CH2OH![]() Cr3+(绿色)+CH3COOH (未配平)
Cr3+(绿色)+CH3COOH (未配平)
(4)基态Cr 原子的价电子排布图为__________________________________
(5)已知Cr3+等过渡元素水合离子的颜色如下表所示:
离子 | Sc3+ | Cr3+ | Fe2+ | Zn2+ |
水合离子的颜色 | 无色 | 绿色 | 浅绿色 | 无色 |
请根据原子结构推测Sc3+、Zn2+的水合离子为无色的原因为________________。
(6)ZnCl2浓溶液常用于除去金属表面的氧化物,例如与FeO反应可得Fe[Zn(OH)Cl2]2溶液。Fe[Zn(OH)Cl2]2的水溶液中不存在的粒子间作用力有____________(填选项字母);
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力 F.氢键
(7)锌是人体必需的微量元素之一,其堆积方式如图1,晶胞结构如图2。锌的堆积方式为_____________________,配位数为_______。