题目内容
15.下列有关物质检验的实验结论正确的是( )| 选项 | 实 验 操 作 及 现 象 | 实 验 结 论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| B | 向某溶液中加入2滴KSCN溶液,溶液不显红色.再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| C | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
| D | 取1mL20%的蔗糖溶液,加入3~5滴稀硫酸,水浴加热5min后,直接加入少量新制备的Cu(OH)2,加热3~5min,没有产生砖红色沉淀 | 说明蔗糖没有水解. |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
分析 A.白色沉淀可能为AgCl;
B.加入2滴KSCN溶液,溶液不显红色,则溶液中不含铁离子,向溶液中加入几滴新制的氯水,溶液变为红色,可知亚铁离子被氧化;
C.氯气等也可使品红褪色;
D.蔗糖水解生成葡萄糖,检验葡萄糖应在碱性溶液中.
解答 解:A.白色沉淀可能为AgCl,则检验硫酸根离子,显加盐酸排除干扰离子,再加氯化钡,故A错误;
B.加入2滴KSCN溶液,溶液不显红色,则溶液中不含铁离子,向溶液中加入几滴新制的氯水,溶液变为红色,可知亚铁离子被氧化,则溶液中一定含Fe2+,故B正确;
C.氯气等也可使品红褪色,则使品红褪色的气体不一定为SO2,故C错误;
D.蔗糖水解生成葡萄糖,检验葡萄糖应在碱性溶液中,则没有加碱至碱性,不能检验葡萄糖,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及离子检验、气体的检验及有机物性质实验等,把握物质的性质、反应原理为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
5.相同物质的量的Na2O2和Na2O的比较中,不正确的是( )
| A. | 所含原子个数之比为4:3 | B. | 所含离子个数之比为4:3 | ||
| C. | 所含氧原子个数之比为2:1 | D. | 所含钠的质量之比为1:1 |
7.下列离子方程式正确的是( )
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+=SO2↑+H2O | |
| B. | CuSO4溶液与过量浓氨水反应的离子方程式:Cu2++2NH3-H2O=Cu(OH)2↓+2NH4+ | |
| C. | 0.01mol/LNH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2 H2O | |
| D. | 向CuSO4溶液中加入Na2O2:2 Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑ |
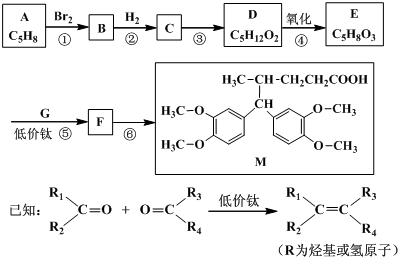
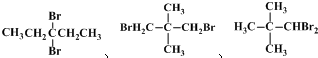 (其中之一);.
(其中之一);.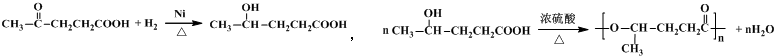 或
或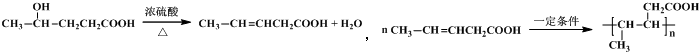 或
或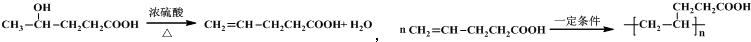 .
.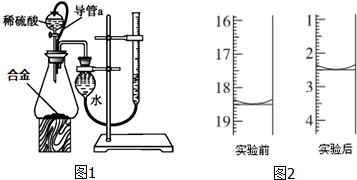 可利用以下方法测定铝镁合金(不含其它元素)组分含量
可利用以下方法测定铝镁合金(不含其它元素)组分含量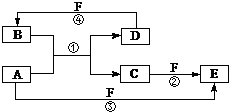 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).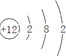 ;反应④的化学方程式为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O.
;反应④的化学方程式为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O. ,反应①的化学方程式为2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
,反应①的化学方程式为2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.