题目内容
7.下列离子方程式正确的是( )| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+=SO2↑+H2O | |
| B. | CuSO4溶液与过量浓氨水反应的离子方程式:Cu2++2NH3-H2O=Cu(OH)2↓+2NH4+ | |
| C. | 0.01mol/LNH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2 H2O | |
| D. | 向CuSO4溶液中加入Na2O2:2 Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑ |
分析 A.发生氧化还原反应生成硫酸钠、NO和水;
B.生成络离子;
C.物质的量比为1:2,反应生成硫酸钡、氢氧化铝和一水合氨;
D.反应生成硫酸钠、氢氧化铜、氧气.
解答 解:A.向稀HNO3中滴加Na2SO3溶液的离子反应为3SO32-+2NO3-+2H+=3SO42-+2NO↑+H2O,故A错误;
B.与过量浓氨水反应,生成络离子,则离子反应为Cu2++4NH3•H2O=[Cu(NH3)4]2++4H2O,故B错误;
C.0.01mol/LNH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合的离子反应为NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3.H2O,故C错误;
D.向CuSO4溶液中加入Na2O2的离子反应为2Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应及络合反应的离子反应考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.下列物质中,属于盐类的是( )
| A. | MgO | B. | NaOH | C. | H2SO4 | D. | BaCO3 |
18.下列既能和稀硫酸反应又能和氢氧化钠溶液反应的化合物是( )
| A. | 氢氧化铁 | B. | 金属铝 | C. | 氧化铝 | D. | 硫酸铜 |
15.下列有关物质检验的实验结论正确的是( )
| 选项 | 实 验 操 作 及 现 象 | 实 验 结 论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| B | 向某溶液中加入2滴KSCN溶液,溶液不显红色.再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| C | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
| D | 取1mL20%的蔗糖溶液,加入3~5滴稀硫酸,水浴加热5min后,直接加入少量新制备的Cu(OH)2,加热3~5min,没有产生砖红色沉淀 | 说明蔗糖没有水解. |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
2.区分下列各组物质的方法不正确的是( )
| A. | 水和双氧水--加二氧化锰 | |
| B. | 二氧化碳和氮气--将燃着的木条伸入瓶中 | |
| C. | 高锰酸钾和二氧化锰--看颜色 | |
| D. | 石灰水和水--通二氧化碳 |
12.下列说法正确的是( )
| A. | 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 | |
| B. | 燃料的脱硫脱氮、SO2的回收利用和NOx的催化转化都是减少酸雨产生的措施 | |
| C. | 要将溶解在CCl4中的碘单质分离出来,可以用蒸馏法,因为碘易升华,先分离出来 | |
| D. | 提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法 |
19.化学与生活、社会密切相关.下列说法不正确的是( )
| A. | 氢氧化铝和碳酸氢钠都可以作为治疗胃酸过多的药剂 | |
| B. | 血液透析是利用了胶体的性质 | |
| C. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| D. | 碘是人体必需微量元素,所以要多吃富含碘单质的食物 |
16.某无色气体可能是H2S,H2,O2,Cl2,NO,NO2,NH3,SO2,CO2中的一种或几种,做实验如下:①若此混合气体通过P2O5无变化,通过浓硫酸有混浊现象,但体积不缩小,剩余气体通过碱石灰,则气体体积缩小到原来的20%,残余气体能燃烧.②若此混合气体通过灼热的铜网,铜网表面变黑,但恢复到原来的温度和压强,体积无变化.③若此混合气体通过装有湿润的有色布条试剂瓶,发现布条不褪色,打开瓶盖也无颜色变化,④若此混合气体通过热的CuSO4溶液时,剩余气体体积为原来的60%,据以上事实,下列说法正确的是( )
| A. | 实验①中通过浓硫酸后气体成分为CO2,H2 | |
| B. | 混合气体中一定含有H2S,H2,CO2,可能有O2 | |
| C. | ②中化学方程式可表示H2S+Cu═CuS+H2 | |
| D. | 把混合气充入轻质气体,待密封好松开手,气球不能自行升空 |
10.据报道,有一种叫Thibacillus Ferroxidans 的细菌在氧气存在下的酸性溶液中,能将黄铜矿(CuFeS2)氧化成硫酸盐,发生的反应为:4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O
(1)CuFeS2中的Fe的化合价为+2,则被氧化的元素为Fe和CuFeS2中的S(填元素名称)
(2)工业生产中利用上述反应后的溶液,按如下流程可制备胆矾(CuSO4•5H2O):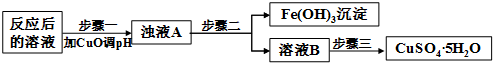
①分析下列表格(其中Ksp是相应金属氢氧化物的沉淀溶解平衡常数):
步骤一应调节溶液的pH范围是3.2≤pH<4.7,请运用沉淀溶解平衡的有关理论解释加入CuO能除去CuSO4溶液中Fe3+的原因加入CuO与H+反应使c(H+)减小,c(OH-)增大,使溶液中c(Fe3+)•c3(OH-)>Ksp[Fe(OH)3],导致Fe3+生成沉淀而除去
②步骤三中的具体操作方法是蒸发浓缩,冷却结晶
(3)工业上冶炼铜的方法之一为:
Cu2S(s)+2Cu2O(s)=6Cu(s)+SO2(g)△H
已知:①2Cu(s)+$\frac{1}{2}$O2(g)=Cu2O(s)△H=-12kJ/mol
②2Cu(s)+S(s)=Cu2S(s)△H=-79.5kJ/mol
③S(s)+O2(g)=SO2(g)△H=-296.8kJ/mol
则该法冶炼铜的反应中△H=-193.3kJ•mol-1.
(1)CuFeS2中的Fe的化合价为+2,则被氧化的元素为Fe和CuFeS2中的S(填元素名称)
(2)工业生产中利用上述反应后的溶液,按如下流程可制备胆矾(CuSO4•5H2O):

①分析下列表格(其中Ksp是相应金属氢氧化物的沉淀溶解平衡常数):
| Ksp | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 2.6×10-39 | 1.9 | 3.2 |
| Cu2+ | 2.2×10-20 | 4.7 | 6.7 |
②步骤三中的具体操作方法是蒸发浓缩,冷却结晶
(3)工业上冶炼铜的方法之一为:
Cu2S(s)+2Cu2O(s)=6Cu(s)+SO2(g)△H
已知:①2Cu(s)+$\frac{1}{2}$O2(g)=Cu2O(s)△H=-12kJ/mol
②2Cu(s)+S(s)=Cu2S(s)△H=-79.5kJ/mol
③S(s)+O2(g)=SO2(g)△H=-296.8kJ/mol
则该法冶炼铜的反应中△H=-193.3kJ•mol-1.