题目内容
5.NH3 通入(即NH3•H2O)AgNO3 溶液反应的化学方程式NH3•H2O+AgNO3=AgOH+NH4NO3,足量氨水与AgNO3 溶液反应的化学方程式2NH3•H2O+AgNO3=[Ag(NH3)2]NO3+2H2O.分析 氨水与足量硝酸银溶液反应生成氢氧化银和硝酸铵,足量氨水与硝酸银溶液反应生成银氨络合溶液,据此解答.
解答 解:氨水与足量硝酸银溶液反应生成氢氧化银和硝酸铵,化学方程式:NH3•H2O+AgNO3=AgOH+NH4NO3;
足量氨水与硝酸银溶液反应生成银氨络合溶液,化学方程式:2NH3•H2O+AgNO3=[Ag(NH3)2]NO3+2H2O;
故答案为:NH3•H2O+AgNO3=AgOH+NH4NO3;2NH3•H2O+AgNO3=[Ag(NH3)2]NO3+2H2O.
点评 本题考查了化学方程式的书写,明确反应实质是解题关键,注意反应物用量对反应的影响,题目难度中等.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
15.下列有关物质检验的实验结论正确的是( )
| 选项 | 实 验 操 作 及 现 象 | 实 验 结 论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| B | 向某溶液中加入2滴KSCN溶液,溶液不显红色.再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| C | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
| D | 取1mL20%的蔗糖溶液,加入3~5滴稀硫酸,水浴加热5min后,直接加入少量新制备的Cu(OH)2,加热3~5min,没有产生砖红色沉淀 | 说明蔗糖没有水解. |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
16.某无色气体可能是H2S,H2,O2,Cl2,NO,NO2,NH3,SO2,CO2中的一种或几种,做实验如下:①若此混合气体通过P2O5无变化,通过浓硫酸有混浊现象,但体积不缩小,剩余气体通过碱石灰,则气体体积缩小到原来的20%,残余气体能燃烧.②若此混合气体通过灼热的铜网,铜网表面变黑,但恢复到原来的温度和压强,体积无变化.③若此混合气体通过装有湿润的有色布条试剂瓶,发现布条不褪色,打开瓶盖也无颜色变化,④若此混合气体通过热的CuSO4溶液时,剩余气体体积为原来的60%,据以上事实,下列说法正确的是( )
| A. | 实验①中通过浓硫酸后气体成分为CO2,H2 | |
| B. | 混合气体中一定含有H2S,H2,CO2,可能有O2 | |
| C. | ②中化学方程式可表示H2S+Cu═CuS+H2 | |
| D. | 把混合气充入轻质气体,待密封好松开手,气球不能自行升空 |
13.元素周期表有多种形式.如图是一种三角形元素素周期表的一部分,下列说法正确的是( )

| A. | M的氧化物易溶于水 | |
| B. | 碳的最简单氢化物的稳定性强于A的 | |
| C. | 钾和B组成的化合物的水溶液显碱性 | |
| D. | A、B形成的化合物中可能含有离子键 |
3.草酸合铁酸钾晶体Kx[Fe(C2O4)y]•3H2O是一种光敏材料,下面是一种制备草酸合铁酸钾晶体的实验流程.
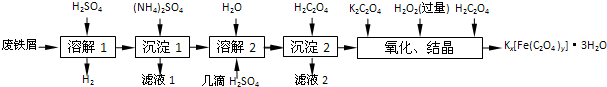
已知:(NH4)2SO4、FeSO4•7H2O、莫尔盐[(NH4)2SO4•FeSO4•6H2O]的溶解度如下表:
(1)“溶解1”应保证铁屑稍过量,其目的是防止Fe2+被氧化为Fe3+.“溶解2”加“几滴H2SO4”的作用是抑制Fe2+水解.
(2)“复分解”制备莫尔盐晶体的基本实验步骤是:蒸发浓缩、冷却结晶、过滤、用乙醇洗涤、干燥.用乙醇洗涤的目的是洗去杂质,减少莫尔盐晶体溶解损失,便于快速干燥.
(3)“沉淀”时得到的FeC2O4•2H2O沉淀需用水洗涤干净.检验沉淀是否洗涤干净的方法是用小试管取少量最后一次洗涤液,加入BaCl2溶液,如出现白色沉淀,说明沉淀没有洗涤干净,否则,沉淀已洗涤干净.
(4)“结晶”时应将溶液放在黑暗处等待晶体的析出,这样操作的原因是黑暗可以防止晶体分解.
(5)请补全测定草酸合铁酸钾产品中Fe3+含量的实验步骤【备选试剂:KMnO4溶液、锌粉、铁粉、NaOH溶液】:
步骤1:准确称取所制备的草酸合铁酸钾晶体a g,配成250mL待测液.
步骤2:用移液管移取25.00mL待测液于锥形瓶中,加入稀H2SO4酸化,加入足量KMnO4溶液,C2O42-转化为CO2被除去.
步骤3:向步骤2所得溶液中加入稍过量的锌粉加热至充分反应(溶液黄色刚好消失),过滤、洗涤、将过滤及洗涤所得溶液收集到锥形瓶中.
步骤4:用c mol•L-1 KMnO4标准溶液滴定步骤3所得溶液至终点,消耗V mL KMnO4标准溶液.

已知:(NH4)2SO4、FeSO4•7H2O、莫尔盐[(NH4)2SO4•FeSO4•6H2O]的溶解度如下表:
| 温度/℃ | 10 | 20 | 30 | 40 | 50 |
| (NH4)2SO4/g | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 |
| FeSO4•7H2O/g | 40.0 | 48.0 | 60.0 | 73.3 | - |
| (NH4)2SO4•FeSO4•6H2O/g | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 |
(2)“复分解”制备莫尔盐晶体的基本实验步骤是:蒸发浓缩、冷却结晶、过滤、用乙醇洗涤、干燥.用乙醇洗涤的目的是洗去杂质,减少莫尔盐晶体溶解损失,便于快速干燥.
(3)“沉淀”时得到的FeC2O4•2H2O沉淀需用水洗涤干净.检验沉淀是否洗涤干净的方法是用小试管取少量最后一次洗涤液,加入BaCl2溶液,如出现白色沉淀,说明沉淀没有洗涤干净,否则,沉淀已洗涤干净.
(4)“结晶”时应将溶液放在黑暗处等待晶体的析出,这样操作的原因是黑暗可以防止晶体分解.
(5)请补全测定草酸合铁酸钾产品中Fe3+含量的实验步骤【备选试剂:KMnO4溶液、锌粉、铁粉、NaOH溶液】:
步骤1:准确称取所制备的草酸合铁酸钾晶体a g,配成250mL待测液.
步骤2:用移液管移取25.00mL待测液于锥形瓶中,加入稀H2SO4酸化,加入足量KMnO4溶液,C2O42-转化为CO2被除去.
步骤3:向步骤2所得溶液中加入稍过量的锌粉加热至充分反应(溶液黄色刚好消失),过滤、洗涤、将过滤及洗涤所得溶液收集到锥形瓶中.
步骤4:用c mol•L-1 KMnO4标准溶液滴定步骤3所得溶液至终点,消耗V mL KMnO4标准溶液.
10.据报道,有一种叫Thibacillus Ferroxidans 的细菌在氧气存在下的酸性溶液中,能将黄铜矿(CuFeS2)氧化成硫酸盐,发生的反应为:4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O
(1)CuFeS2中的Fe的化合价为+2,则被氧化的元素为Fe和CuFeS2中的S(填元素名称)
(2)工业生产中利用上述反应后的溶液,按如下流程可制备胆矾(CuSO4•5H2O):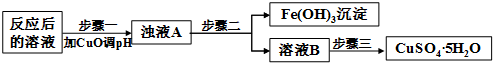
①分析下列表格(其中Ksp是相应金属氢氧化物的沉淀溶解平衡常数):
步骤一应调节溶液的pH范围是3.2≤pH<4.7,请运用沉淀溶解平衡的有关理论解释加入CuO能除去CuSO4溶液中Fe3+的原因加入CuO与H+反应使c(H+)减小,c(OH-)增大,使溶液中c(Fe3+)•c3(OH-)>Ksp[Fe(OH)3],导致Fe3+生成沉淀而除去
②步骤三中的具体操作方法是蒸发浓缩,冷却结晶
(3)工业上冶炼铜的方法之一为:
Cu2S(s)+2Cu2O(s)=6Cu(s)+SO2(g)△H
已知:①2Cu(s)+$\frac{1}{2}$O2(g)=Cu2O(s)△H=-12kJ/mol
②2Cu(s)+S(s)=Cu2S(s)△H=-79.5kJ/mol
③S(s)+O2(g)=SO2(g)△H=-296.8kJ/mol
则该法冶炼铜的反应中△H=-193.3kJ•mol-1.
(1)CuFeS2中的Fe的化合价为+2,则被氧化的元素为Fe和CuFeS2中的S(填元素名称)
(2)工业生产中利用上述反应后的溶液,按如下流程可制备胆矾(CuSO4•5H2O):

①分析下列表格(其中Ksp是相应金属氢氧化物的沉淀溶解平衡常数):
| Ksp | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 2.6×10-39 | 1.9 | 3.2 |
| Cu2+ | 2.2×10-20 | 4.7 | 6.7 |
②步骤三中的具体操作方法是蒸发浓缩,冷却结晶
(3)工业上冶炼铜的方法之一为:
Cu2S(s)+2Cu2O(s)=6Cu(s)+SO2(g)△H
已知:①2Cu(s)+$\frac{1}{2}$O2(g)=Cu2O(s)△H=-12kJ/mol
②2Cu(s)+S(s)=Cu2S(s)△H=-79.5kJ/mol
③S(s)+O2(g)=SO2(g)△H=-296.8kJ/mol
则该法冶炼铜的反应中△H=-193.3kJ•mol-1.
7.向恒温、恒容(2L)的密闭容器中充入2mol SO2和一定量的O2,发生反应:2SO2(g)+O2(g)$\stackrel{一定条件}{?}$2SO3(g);△H=-197.74kJ•mol-1,4min后达到平衡,这时c(SO2)=0.2mol.•L-1,且SO2和O2的转化率相等.下列说法中正确的是( )
| A. | 2min时,c(SO2)=0.6mol•L-1 | |
| B. | 再向容器中充入1mol SO3,达到新平衡,n(SO2):n(SO3)=2:1 | |
| C. | 用O2表示4min内的反应速率为0.1mol•(L•min)-1 | |
| D. | 4min后,若升高温度,平衡向逆方向移动,平衡常数K增大 |