题目内容
【题目】银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电池和照明器材等领域亦有广泛应用。回答下列问题。
(1)久存的银制器皿表面会变黑,失去银白色的光泽,原因是。
(2)已知,Ksp=(AgCl)=1.8×10-10 , 若向50mL0.018mol/L的AgNO3溶液中加入50mL0.020mol/L的盐酸,混合后溶液中的Ag+的浓度为 mol/L,pH为 。
(3)AgNO3溶液光照易分解,生成Ag和红棕色气体等物质,其光照分解的化学方程式为 。
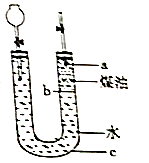
(4)右图所示原电池正极的反应式为 。
【答案】Ag与空气中含硫化合物反应生成黑色硫化银;1.8×10-7mol/L;2;2AgNO3![]() Ag+2NO2 ↑+O2 ↑;Ag++e-=Ag
Ag+2NO2 ↑+O2 ↑;Ag++e-=Ag
【解析】(1)根据金属的腐蚀可知Ag变黑是发生了化学腐蚀,Ag与空气中氧及含硫化合物反应生成黑色硫化银;(2)根据反应中HCl和硝酸银的物质的量可知HCl过量,则计算剩余的氯离子的物质的量浓度为![]() ,根据AgCl的溶度积的表达式计算即可;因该反应中氢离子未参加反应,所以溶液的体积变为100mL时,氢离子的浓度为0.01molL,则pH=2。(3)根据氧化还原反应理论,硝酸银分解生成Ag和二氧化氮气体,无元素化合价升高的,所以该反应中有氧气生成。(4)该原电池的实质是Cu与银离子发生置换反应生成Ag单质,所以正极是生成Ag单质的还原反应。
,根据AgCl的溶度积的表达式计算即可;因该反应中氢离子未参加反应,所以溶液的体积变为100mL时,氢离子的浓度为0.01molL,则pH=2。(3)根据氧化还原反应理论,硝酸银分解生成Ag和二氧化氮气体,无元素化合价升高的,所以该反应中有氧气生成。(4)该原电池的实质是Cu与银离子发生置换反应生成Ag单质,所以正极是生成Ag单质的还原反应。

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3﹣)已成为环境修复研究的热点之一.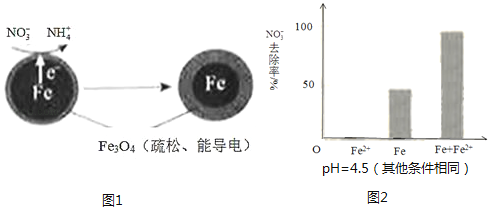
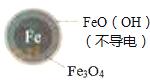
(1)Fe还原水体中NO3﹣的反应原理如图1所示.
①作负极的物质是 .
②正极的电极反应式是 .
(2)将足量铁粉投入水体中,经24小时测定NO3﹣的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3﹣的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3﹣的去除率低.其原因是 .
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3﹣的去除率.对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3﹣;
Ⅱ.Fe2+破坏FeO(OH)氧化层.
①做对比实验,结果如图2所示,可得到的结论是 .
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4 . 结合该反应的离子方程式,解释加入Fe2+提高NO3﹣去除率的原因: .
(4)其他条件与(2)相同,经1小时测定NO3﹣的去除率和pH,结果如表:
初始pH | pH=2.5 | pH=4.5 |
NO3﹣的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始pH不同时,NO3﹣去除率和铁的最终物质形态不同的原因: .
【题目】按要求写出方程式.
(1)碳酸氢铵溶液中加入过NaOH溶液,并加热(写出离子方量程式) .
(2)已知4℃时四种化合物在水中和液氨中的溶解度如表:
AgNO3 | Ba(NO3)2 | AgCl | BaCl2 | |
H2O (液) | 170g | 9.2g | 1.5×10﹣4g | 33.3g |
NH3(液) | 86g | 97.2g | 0.8g | 0g |
上述四种物质在水中形成复分解反应的离子方程式为 , 在液氨中发生复分解反应的化学方程式为 .