题目内容
【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3﹣)已成为环境修复研究的热点之一.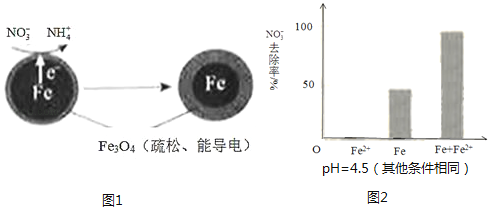
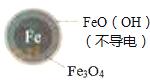
(1)Fe还原水体中NO3﹣的反应原理如图1所示.
①作负极的物质是 .
②正极的电极反应式是 .
(2)将足量铁粉投入水体中,经24小时测定NO3﹣的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3﹣的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3﹣的去除率低.其原因是 .
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3﹣的去除率.对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3﹣;
Ⅱ.Fe2+破坏FeO(OH)氧化层.
①做对比实验,结果如图2所示,可得到的结论是 .
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4 . 结合该反应的离子方程式,解释加入Fe2+提高NO3﹣去除率的原因: .
(4)其他条件与(2)相同,经1小时测定NO3﹣的去除率和pH,结果如表:
初始pH | pH=2.5 | pH=4.5 |
NO3﹣的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始pH不同时,NO3﹣去除率和铁的最终物质形态不同的原因: .
【答案】
(1)铁;NO3﹣+8e﹣+7H2O=NH4++10OH﹣
(2)pH越高,Fe3+越易水解生成FeO(OH),FeO(OH)不导电,所以NO3﹣的去除率低
(3)Ⅱ;Fe2++2FeO(OH)=Fe3O4+2H+ , 加入Fe2+之所以可以提高硝酸根离子的转化率主要因为减少了FeO(OH)的生成,增强了导电性,另外生成了H+ , H+浓度增大,pH减小,使NO3﹣的转化率增大
(4)由于Fe3+的水解,所以pH越高,Fe3+越容易生成FeO(OH),FeO(OH)又不导电,所以NO3﹣的去除率越低
【解析】解:(1)①Fe还原水体中NO3﹣ , 则Fe作还原剂,失去电子,作负极,
故答案为:铁;
②NO3﹣在正极得电子发生还原反应产生NH4+ , 根据电荷守恒写出离子方程式:NO3﹣+8e﹣+7H2O=NH4++10OH﹣ ,
故答案为:NO3﹣+8e﹣+7H2O=NH4++10OH﹣;
(2)pH越高,Fe3+越易水解生成FeO(OH),FeO(OH)不导电,所以NO3﹣的去除率低,
故答案为:pH越高,Fe3+越易水解生成FeO(OH),FeO(OH)不导电,所以NO3﹣的去除率低;
(3)①从右图可以看出只加入铁粉和只加入Fe2+ , NO3﹣的去除率都不及同时加入铁和亚铁离子时NO3﹣的去除率高,说明不是应用了亚铁离子的还原性提高硝酸根的去除率,而是由于Fe2+破坏FeO(OH)氧化层,
故答案为:Ⅱ;
②同位素示踪法证实了Fe2+能与FeO(OH)反应生成Fe3O4 , 离子方程式为:Fe2++2FeO(OH)=Fe3O4+2H+ , 加入Fe2+之所以可以提高硝酸根离子的转化率主要因为减少了FeO(OH)的生成,增强了导电性,另外生成了H+ , H+浓度增大,pH减小,使NO3﹣的转化率增大,
故答案为:Fe2++2FeO(OH)=Fe3O4+2H+ , 加入Fe2+之所以可以提高硝酸根离子的转化率主要因为减少了FeO(OH)的生成,增强了导电性,另外生成了H+ , H+浓度增大,pH减小,使NO3﹣的转化率增大;
(4)由于Fe3+的水解,所以pH越高,Fe3+越容易生成FeO(OH),FeO(OH)又不导电,所以NO3﹣的去除率越低,
故答案为:由于Fe3+的水解,所以pH越高,Fe3+越容易生成FeO(OH),FeO(OH)又不导电,所以NO3﹣的去除率越低.
(1)①Fe还原水体中NO3﹣ , 则Fe作还原剂,失去电子,作负极;②NO3﹣在正极得电子发生还原反应产生NH4+;
(2)pH越高,Fe3+越易水解生成FeO(OH),FeO(OH)不导电,所以NO3﹣的去除率低;
(3)①从右图可以看出只加入铁粉和只加入Fe2+ , NO3﹣的去除率都不及同时加入铁和亚铁离子时NO3﹣的去除率高,说明不是应用了亚铁离子的还原性提高硝酸根的去除率;②同位素示踪法证实了Fe2+能与FeO(OH)反应生成Fe3O4 , 离子方程式为:Fe2++2FeO(OH)=Fe3O4+2H+ , 既减少了FeO(OH)的生成,增强了导电性,又生成了H+ , H+浓度增大,pH减小,使NO3﹣的转化率增大;
(4)由于Fe3+的水解,所以pH越高,Fe3+越容易生成FeO(OH),FeO(OH)又不导电,所以NO3﹣的去除率越低.考查化学反应原理,涉及到的知识有电化学、氧化还原反应等,题中的Fe与NO3﹣的反应跟溶液酸碱性有关,抓住这一点是解题的关键,第Ⅱ问的解答有一定的难度,特别是阐述上的准确性.

 智慧小复习系列答案
智慧小复习系列答案