题目内容
13.下列叙述错误的是( )| A. | 用金属钠可区分乙醇和乙醚 | |
| B. | 用高锰酸钾酸性溶液可区分乙烷和乙烯 | |
| C. | 用水可区分苯和溴苯 | |
| D. | 用裂化汽油从碘水中提取碘 |
分析 A.乙醇含有羟基,可与钠反应生成氢气;
B.乙烯含有碳碳双键,可被氧化;
C.苯和溴苯的密度不同;
D.裂化汽油含有不饱和烃.
解答 解:A.乙醇含有羟基,可与钠反应生成氢气,二乙醚与钠不反应,可鉴别,故A正确;
B.乙烯含有碳碳双键,可被氧化,乙烷与酸性高锰酸钾不反应,可鉴别,故B正确;
C.苯和溴苯的密度不同,苯的密度比水小,溴苯的密度比水大,可鉴别,故C正确;
D.裂化汽油含有不饱和烃,与碘发生加成反应,应用直溜汽油、苯或四氯化碳等萃取,故D错误.
故选D.
点评 本题考查有机物的鉴别,为高频考点,侧重于学生的分析、实验能力的考查,注意把握有机物的性质的异同,难度不大.

练习册系列答案
相关题目
4.下列有关物质性质、结构的表述均正确,且存在因果关系的是( )
| 表述Ⅰ | 表述Ⅱ | |
| A | 在水中,NaCl的溶解度比I2的溶解度大 | NaCl晶体中C1-与Na+间的作用力大于碘晶体中分子间的作用力 |
| B | 通常条件下,CH4分子比PbH4分子稳定性高 | Pb的原子半径比C的大,Pb与H之间的键能比C与H间的小 |
| C | NaCl的熔点比MgO的熔点高 | NaCl的晶格能比MgO的晶格能大 |
| D | P4O10、C6H12O6溶于水后均不导电 | P4O10、C6H12O6均属于共价化合物 |
| A. | A | B. | B | C. | C | D. | D |
1.关于氢键,下列说法正确的是( )
| A. | 水在结冰时体积膨胀,是由于水分子之间存在氢键 | |
| B. | 由于N、O、F的第一电离能较大,所以NH3、H2O、HF分子间可以形成氢键 | |
| C. | 只要有氢键,物质的熔点和沸点就会升高 | |
| D. | H2O是一种非常稳定的化合物,这是由于氢键所致 |
8.下列表示对应化学反应的离子方程式正确的是( )
| A. | 铜和浓硝酸反应:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O | |
| B. | 碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 氢氧化铜溶于硝酸:2H++Cu(OH)2=Cu2++2H2O | |
| D. | 氧化亚铁溶于稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O |
5.在通常条件下,下列各组物质的性质排列不正确的是( )
| A. | 熔点:CO2>KCl>SiO2 | |
| B. | 酸性:HClO4>H2SO4>H3PO4 | |
| C. | 与同浓度的稀盐酸反应剧烈程度:Mg>Al | |
| D. | 热稳定性:HF>H2O>NH3 |
2.下列递变规律正确的是( )
| A. | KOH、Ca(OH)2、Mg(OH)2、Al(OH)3的碱性逐渐增强 | |
| B. | Na、Mg、Al、Si的金属性逐渐增强 | |
| C. | O、S、Na、K的原子半径依次增大 | |
| D. | HF、HCl、H2S、PH3的稳定性依次增强 |
3.下列变化中,不需要破坏化学键的是( )
| A. | 氯化氢溶于水 | B. | 氯化钠溶于水 | C. | 干冰的升华 | D. | 氯化钠熔化 |
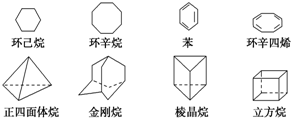 下列是八种环状的烃类物质:
下列是八种环状的烃类物质: