题目内容
18.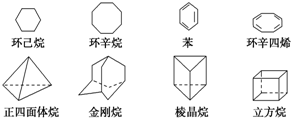 下列是八种环状的烃类物质:
下列是八种环状的烃类物质:(1)互为同系物的有环己烷和环辛烷(填名称),
(2)为同分异构体的有苯和棱晶烷,环辛四烯和立方烷(填写名称,可以不填满,也可以再补充).
(3)正四面体烷的二氯取代产物有1种;立方烷的二氯取代产物有3种;金刚烷的一氯取代产物有2种.
分析 (1)同系物:结构相似,分子组成上相差一个或若干个CH2原子团的化合物;
(2)同分异构体:分子式相同,结构不同的有机物;
(3)根据正四面体烷二氯代物的种类取决于一氯代物中氢原子的种类;立方烷的二氯代物取决于一氯代物中氢原子的种类;金刚烷的一氯代物取决于氢原子的种类.
解答 解:(1)同系物:结构相似,分子组成上相差一个或若干个CH2原子团的化合物,则环己烷(C6H12)与环辛烷(C8H16)均为环烷烃,分子组成上相差2个CH2,互为同系物;
故答案为:环己烷;环辛烷;
(2)同分异构体:分子式相同,结构不同的化合物,则苯与棱晶烷(分子式均为C6H6),环辛四烯与立方烷(分子式均为C8H8)互为同分异构体.
故答案为:苯;棱晶烷;环辛四烯;立方烷;
(3)正四面体烷完全对称,只有一种氢原子,一氯代物只有1种,一氯代物中氢原子也只有1种,所以故二氯代物只有1种;
立方烷分子中只有一种氢原子,其一氯代物有1种,而一氯代物有3种氢原子,分为在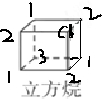 ,则立方烷的二氯代物有3种;
,则立方烷的二氯代物有3种;
金刚烷分子中有两种氢原子,一种是次甲基氢,一种亚甲基氢,所以其一氯代物有2种;
故答案为:1;3;2.
点评 本题主要考查了同系物、同分异构体的判断,限制条件下同分异构体的书写,难度中等,注意同分异构体的种类确定.

练习册系列答案
相关题目
9.已知C3N4晶体具有和金刚石类似的结构,很可能具有比金刚石更大的硬度,且原子间均以单键结合,下列关于C3N4晶体的说法正确的是( )
| A. | C3N4晶体是分子晶体 | |
| B. | C3N4晶体中,C原子采用sp3杂化,氮原子采用sp2杂化 | |
| C. | C3N4晶体中,C-N键的键长比金刚石中的C-C键的键长要短 | |
| D. | C3N4晶体中存在配位键 |
6.下列化学用语正确的是( )
| A. | 原子核内有8个中子的氧原子:18O | B. | Na2O的电子式: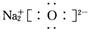 | ||
| C. | CO2的比例模型: | D. | F一的结构示意图: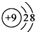 |
13.下列叙述错误的是( )
| A. | 用金属钠可区分乙醇和乙醚 | |
| B. | 用高锰酸钾酸性溶液可区分乙烷和乙烯 | |
| C. | 用水可区分苯和溴苯 | |
| D. | 用裂化汽油从碘水中提取碘 |
3.氯化钠是日常生活中人们常用的调味品.下列性质可以证明氯化钠中一定存在离子键的是( )
| A. | 常温下能溶于水 | B. | 水溶液能导电 | C. | 具有较高的熔点 | D. | 熔融状态能导电 |
7.针对如表9种元素,完成以下各小题
(1)单质为有色气体的元素是氯(填名称).
(2)③与④⑤简单离子的半径由大到小的顺序为O2->Na+>Mg2+(填离子符号).
(3)元素②的单质的电子式为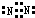 .
.
(4)最高价氧化物对应的水化物酸性最强的是HClO4.(填化学式)
(5)④和⑥的最高价氧化物对应的水化物反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(6)⑦的单质的用途正确的是BD.
A.光导纤维 B.太阳能电池 C.普通玻璃 D.计算机芯片
(7)元素①和⑦非金属性较强的是C,写出一个能表示二者非金属性强弱关系的化学方程式为:Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓.
| 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)③与④⑤简单离子的半径由大到小的顺序为O2->Na+>Mg2+(填离子符号).
(3)元素②的单质的电子式为
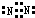 .
.(4)最高价氧化物对应的水化物酸性最强的是HClO4.(填化学式)
(5)④和⑥的最高价氧化物对应的水化物反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(6)⑦的单质的用途正确的是BD.
A.光导纤维 B.太阳能电池 C.普通玻璃 D.计算机芯片
(7)元素①和⑦非金属性较强的是C,写出一个能表示二者非金属性强弱关系的化学方程式为:Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓.
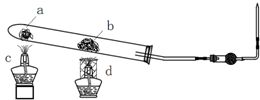
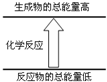 下列变化完全符合如图图示的是
下列变化完全符合如图图示的是