题目内容
1.关于氢键,下列说法正确的是( )| A. | 水在结冰时体积膨胀,是由于水分子之间存在氢键 | |
| B. | 由于N、O、F的第一电离能较大,所以NH3、H2O、HF分子间可以形成氢键 | |
| C. | 只要有氢键,物质的熔点和沸点就会升高 | |
| D. | H2O是一种非常稳定的化合物,这是由于氢键所致 |
分析 A.冰中水分子间形成的氢键,使得水分子间的空隙增大;
B.氢键的形成与非金属性有关;
C.若形成分子内氢键的,其熔点和沸点会降低;
D.氢键只影响物理性质,与化学性质无关.
解答 解:A.在固态水(冰)中,水分子大范围地以氢键互相联结,形成相当疏松的晶体,从而在结构中有许多空隙,造成体积膨胀,故A正确;
B.非金属性较强的元素的氢化物易形成氢键,则NH3、H2O、HF分子间可以形成氢键,与第一电离能无关,故B错误;
C.若形成分子内氢键的,其熔点和沸点会降低,形成分子间氢键时,物质的熔点和沸点就会升高,故C错误;
D.H2O是一种非常稳定的化合物,与共价键有关,与氢键无关,故D错误.
故选A.
点评 本题考查氢键的形成与性质,题目难度不大,注意氢键与分子间作用力、化学键的区别.

练习册系列答案
相关题目
12.中学常见物质A、B、C、D、E、X,存在图中转化关系(部分生成物和反应条件略去).下列推断不正确的是( )


| A. | 若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是氯气 | |
| B. | 若D是一种强碱,则A、B、C均可与X反应生成D | |
| C. | 若D为NaCl,且A可与C反应生成B,则E一定是CO2 | |
| D. | 若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C |
12.用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,下列操作会造成测定结果偏高的原因是( )
| A. | 未用标准液润洗碱式滴定管 | |
| B. | 滴定终点读数时,俯视滴定管的刻度 | |
| C. | 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗 | |
| D. | 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液 |
9.已知C3N4晶体具有和金刚石类似的结构,很可能具有比金刚石更大的硬度,且原子间均以单键结合,下列关于C3N4晶体的说法正确的是( )
| A. | C3N4晶体是分子晶体 | |
| B. | C3N4晶体中,C原子采用sp3杂化,氮原子采用sp2杂化 | |
| C. | C3N4晶体中,C-N键的键长比金刚石中的C-C键的键长要短 | |
| D. | C3N4晶体中存在配位键 |
16.87g MnO2与含HCl为146g的浓盐酸共热在不考虑HCl挥发的情况下得到的Cl2为( )
| A. | 142g | B. | 71g | C. | 小于71 g | D. | 大于142 g |
6.下列化学用语正确的是( )
| A. | 原子核内有8个中子的氧原子:18O | B. | Na2O的电子式: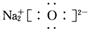 | ||
| C. | CO2的比例模型: | D. | F一的结构示意图: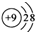 |
13.下列叙述错误的是( )
| A. | 用金属钠可区分乙醇和乙醚 | |
| B. | 用高锰酸钾酸性溶液可区分乙烷和乙烯 | |
| C. | 用水可区分苯和溴苯 | |
| D. | 用裂化汽油从碘水中提取碘 |
11.下列说法正确的是( )
| A. | 常温下,淀粉遇I-变蓝色 | |
| B. | 油脂水解可得到氨基酸和甘油 | |
| C. | 纤维素属于高分子化合物,与淀粉互为同分异构体 | |
| D. | 蛋白质水解的最终产物既能和强酸反应,又能和强碱反应 |