题目内容
17.下列离子方程式与所述事实相符且正确的是( )| A. | 向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 向次氯酸钙溶液中通入过量CO2:2ClO-+Ca2++H2O+CO2═2HClO+CaCO3↓ | |
| C. | 向含0.015 molNaOH的溶液中通入0.64 g SO2:3OH-+2SO2═SO32-+HSO3-+H2O | |
| D. | 向Fe(OH)2中加入足量稀硝酸:Fe(OH)2+2H+═Fe2++2H2O |
分析 A.反应生成氢氧化铝和氯化铵;
B.反应生成碳酸氢钙和HClO;
C.0.64 g SO2的物质的量为0.01mol,NaOH与SO2的物质的量比为3:2,反应生成亚硫酸钠和亚硫酸氢钠;
D.发生氧化还原反应生成硝酸铁、NO和水.
解答 解:A.向氯化铝溶液中加入过量氨水的离子反应为Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故A错误;
B.向次氯酸钙溶液中通入过量CO2的离子反应为ClO-+H2O+CO2═HClO+HCO3-,故B错误;
C.向含0.015 molNaOH的溶液中通入0.64 g SO2的离子反应为3OH-+2SO2═SO32-+HSO3-+H2O,故C正确;
D.向Fe(OH)2中加入足量稀硝酸的离子反应为NO3-+3Fe(OH)2+10H+═3Fe3++NO↑+8H2O,故D错误;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、与量有关的离子反应考查,综合性较强,题目难度不大.

练习册系列答案
相关题目
7.浓度均为0.1mol/L的五种溶液:①CH3COOH ②Ba(OH)2 ③CH3COONa ④NaOH ⑤Na2CO3中,由水电离出的c(H+)按由小到大的排列正确的是( )
| A. | ②④①③⑤ | B. | ④②①⑤③ | C. | ⑤③①④② | D. | ②④⑤①③ |
8.如表是元素周期表的一部分,丙为地壳中含量最高的金属.下列说法不正确的是( )

| A. | 最高价氧化物水化物的酸性:乙<丁 | |
| B. | 甲形成化合物种类最多的元素 | |
| C. | 戊元素位于第4周期第VIIB族 | |
| D. | 乙、丙的最高价氧化物的水化物可以反应 |
5.下列离子方程式正确的是( )
| A. | FeCl3溶液中滴加KSCN溶液:Fe3++3SCN-═Fe(SCN)3↓ | |
| B. | 苯酚钠溶液中通入少量CO2: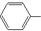 O-+CO2+H2O→ O-+CO2+H2O→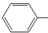 OH+HCO3- OH+HCO3- | |
| C. | NaHCO3溶液中加过量Ca(OH)2溶液:Ca2++2HCO3-+2OH-═CaCO3↓+H2O+CO32- | |
| D. | BaCO3固体中加入足量稀H2SO4:BaCO3+2H+═Ba2++CO2↑+H2O |
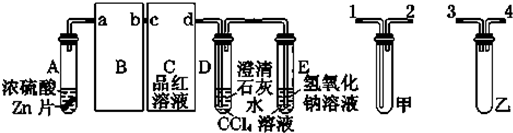
12.下列有关实验装置进行的相应实验,能达到实验目的是( )
| A. |  用图装置萃取溴水中的溴,并把溴的苯溶液从下口放出 | |
| B. |  用图装置可以验证溴乙烷发生了消去反应 | |
| C. |  用图装置配制银氨溶液 | |
| D. |  用图装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |
2.下列有关化学用语表示正确的是( )
| A. | NaOH的电子式: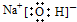 | |
| B. | 质子数和中子数均为16的硫原子:1616S | |
| C. | 氟原子的结构示意图: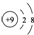 | |
| D. | 乙醛的结构简式: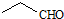 |
9.化学与社会、生产、生活紧切相关.下列说法正确的是( )
| A. | 棉花和木材的主要成分都是纤维素,蚕丝和人造丝的主要成分都是蛋白质 | |
| B. | 石油干馏可得到石油气、汽油、煤油、柴油等 | |
| C. | 从海水中提取物质都必须通过化学反应才能实现 | |
| D. | “地沟油”可用于制肥皂以及生物柴油以达到其再利用 |
2.NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 1.0L1.0mo1•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| B. | 常温常压下,8gO2含有4NA个电子 | |
| C. | 25℃时pH=13的NaOH溶液中含有OH一的数目为0.1NA | |
| D. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |