题目内容
5.下列离子方程式正确的是( )| A. | FeCl3溶液中滴加KSCN溶液:Fe3++3SCN-═Fe(SCN)3↓ | |
| B. | 苯酚钠溶液中通入少量CO2: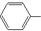 O-+CO2+H2O→ O-+CO2+H2O→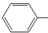 OH+HCO3- OH+HCO3- | |
| C. | NaHCO3溶液中加过量Ca(OH)2溶液:Ca2++2HCO3-+2OH-═CaCO3↓+H2O+CO32- | |
| D. | BaCO3固体中加入足量稀H2SO4:BaCO3+2H+═Ba2++CO2↑+H2O |
分析 A.Fe3+与SCN-反应生成Fe(SCN)3络合物,不是沉淀;
B.碳酸酸性强于苯酚,但苯酚酸性强于碳酸氢根离子,苯酚钠通入二氧化碳生成苯酚和碳酸氢钠;
C.在NaHCO3溶液中加入过量的Ca(OH)2反应生成碳酸钙和氢氧化钠和水;
D.BaCO3固体中加入足量稀H2SO4,生成硫酸钡沉淀水和二氧化碳;
解答 解:A.FeCl3溶液中滴加KSCN溶液:反应的离子方程式是Fe3++3SCN-?Fe(SCN)3,故A错误;
B.碳酸的酸性比苯酚的酸性强,所以苯酚钠通入二氧化碳生成苯酚和碳酸氢钠,反应的化学方程式为:C6H5ONa+CO2+H2O→C6H6OH+NaHCO3,离子反应为:C6H5O-+CO2+H2O→C6H6OH+HCO3-,故B正确;
C.在NaHCO3溶液中加入过量的Ca(OH)2反应生成碳酸钙和氢氧化钠和水,离子方程式:Ca2++HCO3-+OH-═CaCO3↓+H2O,故C错误;
D.BaCO3固体中加入足量稀H2SO4,BaCO3+2H++SO42-═BaSO4↓+CO2↑+H2O,故D错误;
故选B.
点评 本题考查离子方程式的书写,题目难度不大,书写时须注意化学式、离子符号是否正确、电荷是否守恒等.

练习册系列答案
 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
15.将0.2mol/L的醋酸钠溶液与0.1mol/L盐酸等体积混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是( )
| A. | c (Cl-)>c(Ac-)>c(HAc)>c(H+) | B. | c(Ac-)+c(HAc)=0.1mol/L | ||
| C. | c (Na+)>cH+)>c(Ac-)>c(OH-) | D. | c(Na+)+c (H+)=c(Ac-)+c(Cl-)+c(OH-) |
20.化学与社会息息相关,下列物质在社会、生活中的应用及解释都正确的是( )
| 选项 | 应用 | 解释 |
| A | 高纯硅作计算机芯片的材料 | 硅晶体在自然界中能稳定存在 |
| B | 在入海口的钢铁闸门上装一定数量的锌块防止闸门被腐蚀 | 利用外加电流的阴极保护法保护金属 |
| C | 高铁车厢采用铝合金材料 | 铝合金强度大,质量轻,不与氧气反应 |
| D | 用浸泡过高锰酸钾溶液的硅藻土保鲜水果 | 其作用是吸收水果释放出的乙烯 |
| A. | A | B. | B | C. | C | D. | D |
17.下列离子方程式与所述事实相符且正确的是( )
| A. | 向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 向次氯酸钙溶液中通入过量CO2:2ClO-+Ca2++H2O+CO2═2HClO+CaCO3↓ | |
| C. | 向含0.015 molNaOH的溶液中通入0.64 g SO2:3OH-+2SO2═SO32-+HSO3-+H2O | |
| D. | 向Fe(OH)2中加入足量稀硝酸:Fe(OH)2+2H+═Fe2++2H2O |
10.下列反应的产物一定是纯净物的是( )
| A. | 丙烯加聚 | B. | 丙烯与水加成 | C. | 丙烯与Br2加成 | D. | 丙烷与Br2光取代 |

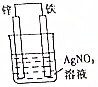 原电池原理的发现是储能和功能技术的巨大进步,是化学对人类的一项重大贡献.
原电池原理的发现是储能和功能技术的巨大进步,是化学对人类的一项重大贡献.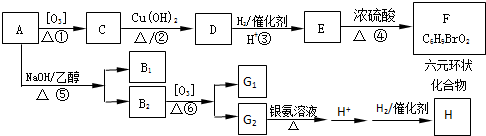
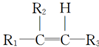
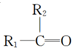 +
+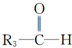
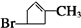

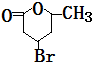 +H2O
+H2O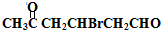 +2Cu(OH)2+NaOH
+2Cu(OH)2+NaOH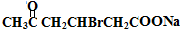 +Cu2O↓+3H2O
+Cu2O↓+3H2O