题目内容
2.NA为阿伏伽德罗常数的值,下列叙述正确的是( )| A. | 1.0L1.0mo1•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| B. | 常温常压下,8gO2含有4NA个电子 | |
| C. | 25℃时pH=13的NaOH溶液中含有OH一的数目为0.1NA | |
| D. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
分析 A.NaAlO2水溶液中,水和偏铝酸钠都含有氧原子;
B.氧气分子中含有16个电子,8g氧气的物质的量为0.25mol,含有4mol电子;
C.溶液体积不知不能计算微粒数;
D.氮气和一氧化碳的摩尔质量都是28g/mol,且都是双原子分子.
解答 解:A.NaAlO2水溶液中,水和偏铝酸钠都含有氧原子,所以1.0L1.0mo1•L-1的NaAlO2水溶液中含有的氧原子数无法计算,故A错误;
B.8g氧气的物质的量为:$\frac{8g}{32g/mol}$=0.25mol,0.25mol氧气中含有电子的物质的量为:16×0.25mol=4mol,含有4NA个电子,故B正确;
C.溶液体积不知,无法计算溶液中氢氧化钠的物质的量,故C错误;
D.14g氮气和CO的混合气体的物质的量为:$\frac{14g}{28g/mol}$=0.5mol,含有原子的物质的量为1mol,含有的原子数目为NA,故D正确;
故选BD.
点评 本题考查了阿伏伽德罗常数的应用,题目难度中等,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,C为易错点,注意明确题中缺少溶液体积,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
相关题目
17.下列离子方程式与所述事实相符且正确的是( )
| A. | 向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 向次氯酸钙溶液中通入过量CO2:2ClO-+Ca2++H2O+CO2═2HClO+CaCO3↓ | |
| C. | 向含0.015 molNaOH的溶液中通入0.64 g SO2:3OH-+2SO2═SO32-+HSO3-+H2O | |
| D. | 向Fe(OH)2中加入足量稀硝酸:Fe(OH)2+2H+═Fe2++2H2O |
13.下表中的数据是破坏或生成1mol物质中的化学键所消耗或吸收的能量(单位:kJ):
根据上述数据回答:
(1)下列氢化物中最稳定的是A(填序号).
A.HCl B.HRr C.HI
(2)有表中数据推知反应I2+H2=2HI释放能量(填“吸收”或“释放”).
(3)相同条件下,X2(X代表Cl、Rr、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的能量最多的是Cl2(填化合物的方程式).
(4)若无上表中的数据,你能正确回答出问题(3)吗?
答:能(填“能”或“不能”);简述你的理由同主族元素按I、Br、Cl的顺序原子得电子能力渐强,生成的HX越趋稳定,相应释放出能量越多.
根据上述数据回答:
| 物质 | Cl2 | Rr2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
A.HCl B.HRr C.HI
(2)有表中数据推知反应I2+H2=2HI释放能量(填“吸收”或“释放”).
(3)相同条件下,X2(X代表Cl、Rr、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的能量最多的是Cl2(填化合物的方程式).
(4)若无上表中的数据,你能正确回答出问题(3)吗?
答:能(填“能”或“不能”);简述你的理由同主族元素按I、Br、Cl的顺序原子得电子能力渐强,生成的HX越趋稳定,相应释放出能量越多.
10.下列反应的产物一定是纯净物的是( )
| A. | 丙烯加聚 | B. | 丙烯与水加成 | C. | 丙烯与Br2加成 | D. | 丙烷与Br2光取代 |
14.下列性质的递变中,正确的是( )
| A. | O、Na、S的原子半径依次增大 | B. | LiOH、KOH、CsOH的碱性依次增强 | ||
| C. | HF、NH3、SiH4的稳定性依次增强 | D. | HCl、HBr、HI的还原性依次减弱 |
11.在一定温度下,体积为2L的容器内M、N的物质的量随时间变化的曲线如图所示,下列说法正确( )


| A. | 反应方程式为N?2M | |
| B. | t2时,正逆反应速率相等 | |
| C. | 其他条件不变,缩小容器的体积,反应速率会加快 | |
| D. | 若t1=1,则0~t1时间段N的平均速率为3mol/(L•min) |
12.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 常温下,0.1 mol•L-1醋酸钠溶液中含有Na+和CH3COO-的总数为0.2NA | |
| B. | 常温下,将0.1 mol铁片放入足量浓硝酸中反应后,转移电子的数目为0.3NA | |
| C. | 2 g NO2和44 g N2O4的混合气体中所含原子的总数为3NA | |
| D. | 0.1 mol甘油醛中含有双键的数目为0.3NA |
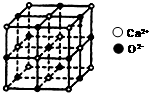 (1)AlN的晶体结构与单晶硅相似,在AlN晶体中,每个Al原子与4个N原子相连,与N元素同主族的元素As位于元素周期表的第四周期,其基态原子的核外电子排布式为1s22s22p63s23p63d104s24p3.
(1)AlN的晶体结构与单晶硅相似,在AlN晶体中,每个Al原子与4个N原子相连,与N元素同主族的元素As位于元素周期表的第四周期,其基态原子的核外电子排布式为1s22s22p63s23p63d104s24p3.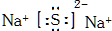 .
.