题目内容
6.0.5L AlCl3溶液中Cl-为9.03×1022个,则AlCl3溶液的物质的量浓度为( )| A. | 0.1 mol•L-1 | B. | 1 mol•L-1 | C. | 3 mol•L-1 | D. | 1.5 mol•L-1 |
分析 n(Cl-)=$\frac{9.03×1{0}^{22}}{6.02×1{0}^{23}/mol}$=0.15mol,每个氯化铝化学式中含有3个氯离子,则n(AlCl3)=$\frac{1}{3}$n(Cl-)=$\frac{1}{3}$×0.15mol=0.05mol,根据c=$\frac{n}{V}$计算氯化铝物质的量浓度.
解答 解:n(Cl-)=$\frac{9.03×1{0}^{22}}{6.02×1{0}^{23}/mol}$=0.15mol,每个氯化铝化学式中含有3个氯离子,则n(AlCl3)=$\frac{1}{3}$n(Cl-)=$\frac{1}{3}$×0.15mol=0.05mol,c(AlCl3)=$\frac{n}{V}$=$\frac{0.05mol}{0.5L}$=0.1mol/L,故选A.
点评 本题考查物质的量有关计算,为高频考点,侧重考查学生计算能力,明确各个物理量关系是解本题关键,注意氯化铝和氯离子个数关系,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.下列离子组在给定条件下,离子共存判断及反应的离子方程式均正确的是( )
| 选项 | 条 件 | 离子组 | 离子共存判断及离子方程式 |
| A | 常温下,由水电离出的C(H+)为1×10-12 mol•L-1 | K+、Cl-、S2-SO32- | 一定能大量共存 |
| B | 滴加氨水 | Na+、Fe3+、Cl- | 不能大量共存 Fe3++3OH-═Fe(OH)3↓ |
| C | p=1的溶液 | Fe3+、I- Cl- | 不能大量共存 2Fe3++2I-═2Fe2++I2 |
| D | 通入少量SO2气体 | K+、Na+、ClO- | 不能大量共存 2ClO-+SO2+H2O═2HClO+SO32- |
| A. | A | B. | B | C. | C | D. | D |
14.某烃的分子量为84,可使酸性高锰酸钾溶液褪色,该烃的链状且主链上有4个碳原子的同分异构体的数目是( )(不考虑顺反异构)
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
1.下列叙述错误的是( )
| A. | 将10gNaCl晶体溶入90g水中,制得10%的NaCl溶液 | |
| B. | 将40gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为1mol/L | |
| C. | 将wga%的NaCl溶液蒸发掉$\frac{w}{2}$g水,得到2a%的NaCl溶液 | |
| D. | 将1体积c1mol/L的硫酸用水稀释为5体积,稀溶液的浓度为0.2 c1mol/L |
 O
O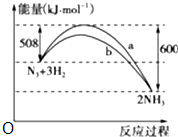 常温下,体积相同pH相同的盐酸和醋酸,同时加入足量表面积相同的锌粒,反应刚开始时反应速率盐酸等于醋酸,反应开始后,反应速率盐酸小于醋酸,反应结束时,产生氢气盐酸小于醋酸.(填大于、小于或等于)
常温下,体积相同pH相同的盐酸和醋酸,同时加入足量表面积相同的锌粒,反应刚开始时反应速率盐酸等于醋酸,反应开始后,反应速率盐酸小于醋酸,反应结束时,产生氢气盐酸小于醋酸.(填大于、小于或等于)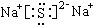 ,
,