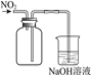题目内容
【题目】下列离子方程式书写正确的是
A.标准状况下2.24LCO2通入1mol/L100mLNaOH溶液中:CO2+OH-→HCO3-
B.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+→Fe3++3H2O
C.Na2S水解:S2-+2H2O![]() H2S+2OH-
H2S+2OH-
D.等物质的量的NH4HCO3与NaOH在溶液中反应:NH4++HCO3-+2OH-→CO32-+NH3+2H2O
【答案】A
【解析】
A.标准状况下2.24LCO2的物质的量为0.1mol,1mol/L100mLNaOH溶液中n(NaOH)=0.1mol,二者1:1完全反应生成碳酸氢钠,离子反应为CO2+OH-=HCO3-,故A正确;
B.碘离子具有还原性,铁离子具有氧化性,二者发生氧化还原反应生成亚铁离子和单质碘,氢氧化铁溶于氢碘酸中的离子反应为2Fe(OH)3+2I-+6H+=2Fe2++I2+6H2O,故B错误;
C. H2S属于二元弱酸,电离分步进行;Na2S属于二元弱酸形成的盐,水解分步进行:S2-+H2O![]() HS-+OH-,HS-+H2O
HS-+OH-,HS-+H2O![]() H2S+ OH-,不能一步到位,故C错误;
H2S+ OH-,不能一步到位,故C错误;
D. 等物质的量的NH4HCO3与NaOH在溶液中反应:HCO3-+OH-=CO32-+ H2O,故D错误;
故答案选A。

练习册系列答案
相关题目
【题目】下列实验装置(部分夹持装置已略去)可以达到对应实验目的的是( )
A | B | C | D | |
实验目的 | 制备氢氧化铁胶体 | 分离乙酸乙酯和饱和Na2CO3溶液 | 除去CO2中的少量HCl | 收集NO2 |
实验装置 |
|
|
|
|
A.AB.BC.CD.D