题目内容
3.工业上制取CuCl2的生产流程如图: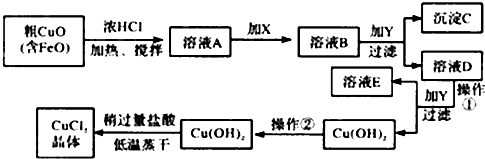
请结合表数据,回答下列问题:
| 物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
②在溶液B中加入试剂Y常见的有:CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3等,调节PHB,(A.PH≥9.6 B.PH 3~4 C.PH≥6.4)其作用是使Fe3+完全转变为氢氧化铁沉淀而分离Fe3+
③往Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2.采用“稍多量盐酸”和“低温蒸干”的目的是抑制 Cu2+水解.
分析 粗氧化铜中含有FeO加入浓HCl加热搅拌得到溶液A,加入氧化剂把亚铁离子氧化为铁离子,加入CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3 等调节溶液PH3-4使铁离子全部沉淀,铜离子不沉淀,得到溶液D,继续加入CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3 等调节溶液PH≥6.4得到氢氧化铜沉淀,过滤得到溶液E和氢氧化铜沉淀,洗涤干燥得到的氢氧化铜就稍过量的盐酸低温蒸干得到氯化铜晶体;
(1)次氯酸钠具有氧化性,由于Fe2+沉淀时Cu2+已基本沉淀完全,所以必须先将Fe2+转变为Fe3+才能完全除去;
(2)加入氧化铜,调节溶液的PH,除去铁离子杂质;
(3)根据平衡Cu2++2H2O?Cu(OH)2+2H+进行分析.
解答 解:粗氧化铜中含有FeO加入浓HCl加热搅拌得到溶液A,加入氧化剂把亚铁离子氧化为铁离子,加入CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3 等调节溶液PH3-4使铁离子全部沉淀,铜离子不沉淀,得到溶液D,继续加入CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3 等调节溶液PH≥6.4得到氢氧化铜沉淀,过滤得到溶液E和氢氧化铜沉淀,洗涤干燥得到的氢氧化铜就稍过量的盐酸低温蒸干得到氯化铜晶体;
(1)根据表中完全沉淀时的pH范围可知,Fe2+沉淀时Cu2+已基本沉淀完全,所以必须先将Fe2+转变为Fe3+才能完全除去,所以溶液A中加入NaClO溶液,目的是氧化Fe2+ 生成Fe3+ 有利于沉淀分离,反应的离子方程式为:2H++ClO-+2 Fe2+=2 Fe3++Cl-+H2O,
故答案为:NaClO;氧化Fe2+生成Fe3+ 有利于沉淀分离;
(2)在溶液B中加CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3等调节溶液的pH使Fe3+完全沉淀,根据表中数据,Fe3+完全沉淀时PH的范围是3~4,
故答案为:Cu2(OH)2CO3;B;使Fe3+完全转变为氢氧化铁沉淀而分离Fe3+;
(3)因为溶液中存在以下平衡:Cu2++2H2O?Cu(OH)2+2H+,加入过量盐酸和低温,能使平衡逆移,防止Cu2+水解,故答案为:抑制 Cu2+水解.
点评 本题以工业上制取CuCl2的生产流程为背景,综合考查学生灵活运用元素化合物知识、氧化还原反应知识、沉淀转化、盐类水解以及实验分析等知识和技能,难度较大.

 全能练考卷系列答案
全能练考卷系列答案Ⅰ.配制偏钒酸钠(NaVO3)溶液
(1)向V2O5 固体中缓慢滴加NaOH溶液,边加热边搅拌至V2O5 固体完全溶解,反应的离子方程式为V2O5+2OH-=2VO3-+H2O.
Ⅱ.沉钒
一定条件下向偏钒酸钠溶液中加入氯化铵溶液,加热、搅拌得到偏钒酸铵沉淀.如图为部分因素对沉钒率的影响.
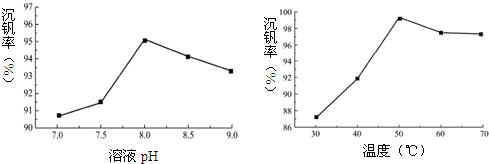
(2)为了提高沉钒率,应调节溶液pH=8.0.已知偏钒酸铵微溶于冷水,可溶于热水,结合图中信息,生成偏钒酸铵沉淀的反应是吸热(填“吸热”或“放热”)反应.
(3)该课题组对影响沉钒率的其他因素(除温度和pH)提出如下假设.
假设一:氯化铵溶液的浓度
假设二:偏钒酸钠溶液浓度
…
(4)结合上述最佳条件设计实验验证假设一,写出实验步骤与结论.
限选试剂:0.5mol/L的偏钒酸钠溶液、1mol/L的氯化铵溶液、蒸馏水,常见实验仪器任选.(提示:沉钒率可用专用仪器测定并计算)
| 实验步骤与结论: |
(5)偏钒酸铵灼烧产生五氧化二钒,该反应的化学方程式为2NH4VO3$\frac{\underline{\;△\;}}{\;}$2NH3↑+H2O↑+V2O5.
| A. | H2O和HNO3 | B. | NaCl和NH3 | C. | CaF2和CsF | D. | Cl2和O2 |
| A. | 明矾可用作净水剂 | B. | 甲醛可用作食品防腐剂 | ||
| C. | 晶体硅可用于制造光导纤维 | D. | 铝制容器可长期存放酸性食物 |
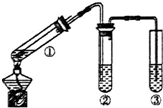
| A. | 上下移动①中铜丝可控制生成SO2的量 | |
| B. | ②中选用品红溶液验证SO2的生成 | |
| C. | ③中选用NaOH溶液吸收多余的SO2 | |
| D. | 该反应中浓硫酸表现了强氧化性和脱水性 |
| A. | 14C与14N含有相同的中子数 | |
| B. | H、D、T互为同位素 | |
| C. | 14C与C60中普通碳原子的化学性质相同 | |
| D. | 14C与12C互为同位素 |
| A. | XY2 | B. | X2Y3 | C. | X2Y | D. | XY |
 和
和 ⑤40K和40Ca ⑥
⑤40K和40Ca ⑥ 与
与 ⑦甲烷与C3H8.
⑦甲烷与C3H8.