题目内容
19.下列各组物质中,互为同位素的是③;互为同素异形体的是①;互为同系物的是⑦;互为同分异构体的是⑥;为同种物质的是②④.(填序号)①O2和O3②H2O和D2O ③37Cl和35Cl ④
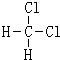 和
和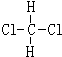 ⑤40K和40Ca ⑥
⑤40K和40Ca ⑥ 与
与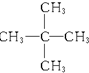 ⑦甲烷与C3H8.
⑦甲烷与C3H8.
分析 同系物指结构相似、通式相同,组成上相差1个或者若干个CH2原子团的化合物,官能团数目和种类相等;
具有相同分子式而结构不同的化合物互为同分异构体;
同种元素形成的不同单质互为同素异形体;
质子数相同质量数(或中子数)不同的原子互称同位素;
组成和结构都相同的物质为同一物质,同一物质组成、结构、性质都相同,结构式的形状及物质的聚集状态可能不同.
解答 解:①O2和O3是由氧元素组成的不同单质,互为同素异形体;
②H2O和D2O都是氢元素和氧元素组成的,结构相同,属于同一物质;
③37Cl和35Cl中子数不同,是氯元素的不同核素,互为同位素;
④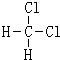 和
和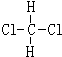 名称与结构简式一致,为同一种物质;
名称与结构简式一致,为同一种物质;
⑥ 与
与 分子式相同,结构不同,为碳链异构,互为同分异构体;
分子式相同,结构不同,为碳链异构,互为同分异构体;
⑦甲烷与C3H8结构相似,都属于烷烃,形成2个CH2原子团,互为同系物.
故答案为:③;①;⑦;⑥;②④.
点评 本题考查同系物、同分异构体、同位素、同素异形体、同一物质的区别,难度不大,注意把握概念的内涵与外延.

练习册系列答案
相关题目
9.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列各项的事实不能说明上述观点的是( )
| A. | 乙烯能发生加成反应,而乙烷不能发生加成反应 | |
| B. | 甲苯能使酸性高锰酸钾溶液褪色,而甲烷不能使酸性高锰酸钾溶液褪色 | |
| C. | 乙基对羟基的影响,使羟基的活性变弱,电离H+的能力不及H2O | |
| D. | 苯酚中的羟基氢能与NaOH溶液反应,而醇羟基氢不能与NaOH溶液反应 |
10.下列各组物质中,一定互为同系物的是( )
| A. | 乙烷和己烷 | B. | CH3COOH、C3H6O2 | C. |  和 和 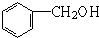 | D. | HCHO、CH3COOH |
7.下列反应属于吸热反应的是( )
①二氧化碳与赤热的炭反应生成一氧化碳
②液态水汽化
③锌粒与稀H2SO4反应制取H2
④Ba(OH)2•8H2O固体与NH4Cl固体反应
⑤生石灰跟水反应.
①二氧化碳与赤热的炭反应生成一氧化碳
②液态水汽化
③锌粒与稀H2SO4反应制取H2
④Ba(OH)2•8H2O固体与NH4Cl固体反应
⑤生石灰跟水反应.
| A. | ①②④ | B. | ①⑤ | C. | ①③④⑤ | D. | ①④ |
14.元素周期表中某一区域的一些元素有着某些相似的用途,可以研发新材料或新药物,下列说法可能错误的是( )
| A. | 在金属与非金属分界处寻找半导体材料 | |
| B. | 在周期表的左上方区域开发新核能 | |
| C. | 在右上方活泼非金属区域寻找新药物 | |
| D. | 在过渡元素区域寻找催化剂和耐高温、耐腐蚀的新材料 |
4.NA为阿伏加德罗常数,下列叙述错误的是( )
| A. | 18gD2O中含的质子数为9 NA | |
| B. | 1.00molNaCl中,所有Na+的最外层电子总数为10×6.02×1023 | |
| C. | 46gNO2和N2O4混合气体中含有原子总数为3 NA | |
| D. | 1molNa 与足量O2 反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
11.除去镁粉中的少量铝粉,可以选用的试剂是( )
| A. | 硫酸溶液 | B. | 氨水溶液 | C. | 盐酸溶液 | D. | 氢氧化钠溶液 |
8.某烃的组成为C15H24,分子结构非常对称.有关实验证明该烃中仅存在三种基团:乙烯基(-CH=CH2),亚甲基(-CH2-)和次甲基(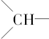 ),并且乙烯基和次甲基之间必须通过亚甲基相连.当该烃含有单环结构时,分子中的乙烯基和亚甲基数依次为( )
),并且乙烯基和次甲基之间必须通过亚甲基相连.当该烃含有单环结构时,分子中的乙烯基和亚甲基数依次为( )
 ),并且乙烯基和次甲基之间必须通过亚甲基相连.当该烃含有单环结构时,分子中的乙烯基和亚甲基数依次为( )
),并且乙烯基和次甲基之间必须通过亚甲基相连.当该烃含有单环结构时,分子中的乙烯基和亚甲基数依次为( )| A. | 4、6 | B. | 2、3 | C. | 3、6 | D. | 3、3 |
3.工业上制取CuCl2的生产流程如图:
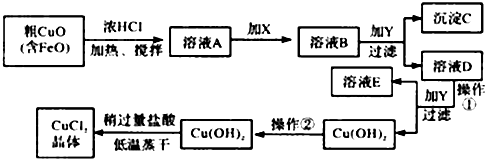
请结合表数据,回答下列问题:
①溶液A中加入X是一种“绿色”氧化剂,则X是NaClO(填化学式),其目的是氧化Fe2+生成Fe3+ 有利于沉淀分离.
②在溶液B中加入试剂Y常见的有:CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3等,调节PHB,(A.PH≥9.6 B.PH 3~4 C.PH≥6.4)其作用是使Fe3+完全转变为氢氧化铁沉淀而分离Fe3+
③往Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2.采用“稍多量盐酸”和“低温蒸干”的目的是抑制 Cu2+水解.

请结合表数据,回答下列问题:
| 物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
②在溶液B中加入试剂Y常见的有:CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3等,调节PHB,(A.PH≥9.6 B.PH 3~4 C.PH≥6.4)其作用是使Fe3+完全转变为氢氧化铁沉淀而分离Fe3+
③往Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2.采用“稍多量盐酸”和“低温蒸干”的目的是抑制 Cu2+水解.