题目内容
工业生产纯碱的工艺流程示意图如下: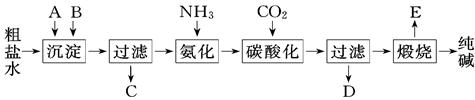
完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式A. ,B.
(2)实验室提纯粗盐的实验操作依次为:取样、 、沉淀、 、 、冷却结晶、 、烘干
(3)工业生产纯碱工艺流程中,碳酸化时产生的现象是 .碳酸化时没有析出碳酸钠晶体,其原因是
(4)碳酸化后过滤、滤液D最主要的成分是 (填写化学式),检验这一成分的阴离子的具体方法是
(5)氨碱法流程中氨是循环使用的,为此,滤液D加入石灰水产生氨.加石灰水后所发生的反应的离子方式程为 ,滤液D加石灰水前先要加热,原因是
(6)产品纯碱中含有碳酸氢钠.如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为 (注明你的表达式中所用的有关符号的含义)
(1)Ca(OH)2或CaO Na2CO3
(2)溶解 过滤 蒸发 过滤
(3)有晶体析出(或出现浑浊) 碳酸钠溶解度比碳酸氢钠大
(4)NH4Cl 取样,加硝酸酸化,再加入硝酸银溶液,有白色沉淀产生,证明该阴离子是氯离子
(5)NH4++OH-=NH3↑+H2O 防止加石灰水时产生碳酸钙沉淀
(6)w(NaHCO3)=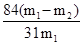 (设加热前质量为m1,加热后m2 )
(设加热前质量为m1,加热后m2 )
解析试题分析:(1)粗盐水中含有Mg2+ 、Ca2+ 、用Ca(OH)2或CaO将Mg2+ 转化为Mg(OH)2 ,再用Na2CO3将Ca2+ 转化为CaCO3沉淀,答案:Ca(OH)2或CaO Na2CO3
⑵实验室提纯粗盐的整个操作过程为:取样、溶解、沉淀、过滤、蒸发、冷却结晶、过滤、烘干几步;答案为:溶解 过滤 蒸发 过滤
(3)纯碱生产中碳酸化时,会看到溶液中析出晶体,这是由于碳酸钠的溶解度大于碳酸氢钠,故答案为:碳酸钠溶解度比碳酸氢钠大;
(4)根据操作过程,氨化后通入二氧化碳的溶液发生复分解反应:H2O+CO2+NH3+NaCl=NaHCO3+NH4Cl,最终得到NH4Cl还有NaHCO3等,碳酸氢钠溶解度很小而结晶,故酸化后滤液的主要成分为:NH4Cl;检验其中的Cl―离子时,要经过取样,加硝酸酸化,加硝酸银,有白色沉淀,该阴离子是氯离子,答案:NH4Cl 取样,加硝酸酸化,再加入硝酸银溶液,有白色沉淀产生,证明该阴离子是氯离子。
(5)滤液中主要含有的是氯化铵,其和石灰水反应时:NH4++OH- NH3↑+H2O,滤液D加石灰水前先要加热,原因是防止加石灰水时产生碳酸钙沉淀,答案为:NH4++OH-
NH3↑+H2O,滤液D加石灰水前先要加热,原因是防止加石灰水时产生碳酸钙沉淀,答案为:NH4++OH- NH3↑+H2O,防止加石灰水时产生碳酸钙沉淀
NH3↑+H2O,防止加石灰水时产生碳酸钙沉淀
(6)假设加热前纯碱的质量为m1,加热后的质量为m2,则加热损失的质量为:m1-m2,则纯碱中碳酸氢钠的质量为: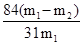 ;故纯碱中含有的碳酸氢钠的质量分数为=
;故纯碱中含有的碳酸氢钠的质量分数为=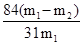 ,答案为:w(NaHCO3)=
,答案为:w(NaHCO3)=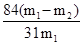 (设加热前质量为m1,加热后m2 )
(设加热前质量为m1,加热后m2 )
考点:纯碱工业(侯氏制碱法)

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案重晶石矿(主要成分为硫酸钡)因为含有Fe2O3、MnO及炭质等杂质而常呈深褐色。工业上将重晶石矿粉碎后与硫酸、铝粉在反应槽中混合加热(即“漂白”),再经水洗等一系列工序制得白色的重晶石填料,广泛用作纸张、油漆等的填充剂。已知MnO是碱性氧化物,Al粉可以将深色的Fe3+转化为浅色的Fe2+。
重晶石填料的生产工艺流程为:
(1)在该流程中,为加快“漂白”速度,采取的措施有 、
。
(2)硫酸起到了“漂白”的作用。请写出硫酸直接起到该作用时的化学方程式:
、 。
(3)二次漂白水洗过滤后,检验滤渣不含Fe2+离子的方法是
、 。
(4)二次漂白前,煅烧的主要目的是 。将煅烧后的固体磨成细粉,使用的是加有刚玉球的振动磨。这说明刚玉具有很高的 。
(5)工业生产中为了充分利用资源,将滤液经过处理得到化工原料Fe2O3。操作过程是:
①滤液中通入过量Cl2,其目的是 。
②再加入适量NaOH来调节溶液的pH ,其目的是 ,调节溶液的pH范围为 。
有关离子开始沉淀及完全沉淀时的pH如下:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
(6)最后通过 、 得到氧化铁。
铁及其化合物有重要用途,如聚合硫酸铁[Fe2(OH)n(SO4)3-n/2]m是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某化学探究小组设计如下方案制备上述两种产品: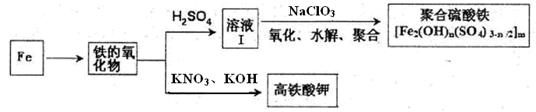
请回答下列问题:
(1)检验固体铁的氧化物中铁的化合价,应使用的试剂是 (填标号)
| A.稀硫酸 | B.稀硝酸 | C.KSCN溶液 | D.酸性高锰酸钾溶液 |
(3)Fe2O3与KNO3和KOH的混合物加热共融可制得高铁酸鉀。完成并配平下列化学方程式:
□Fe2O3+□KNO3+□KOH——□ +□KNO2+□ 。
(4)为测定溶液I中铁元素的总含量,实验操作:准确量取20.00mL溶液I于带塞锥形瓶中,加入足量H2O2,调节pH<3,加热除去过量H2O2;加入过量KI充分反应后,再用 0.1000mol·L—1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。
已知:2Fe3++2I—=2Fe2++I2、I2+2S2O32—=2I—+S4O62—。
①写出滴定选用的指示剂 ,滴定终点观察到的现象 。
②溶液I中铁元素的总含量为 g·L—1。若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会 (填“偏高”、“偏低”、“不变”)。
某氧化铁样品中含有少量的FeSO4杂质。某同学要测定其中铁元素的质量分数,他设计了如下方案进行测定,操作流程为: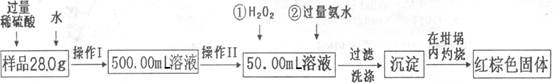
请根据流程回答:
(1)操作I中配制溶液时,所用到的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管以外,还必须有 (填仪器名称)。
(2)操作II中必须用到的仪器是 。
| A.50mL量筒 | B.100mL量筒 |
| C.50mL酸式滴定管 | D.50mL碱式滴定管 |
(4)检验沉淀中SO42-是否冼涤干净的操作
。
(5)将沉淀物加热,冷却至室温,用天平称量坩埚与加热后固体的总质量为blg,再次加热并冷却至室温称量其质量为b2g,若b1—b2=0.3,还应进行的操作是
。
(6)若坩埚的质量为42.6g,最终坩埚与加热后同体的总质量为44.8g,则样品中铁元素的质量分数= (保留一位小数)。
(7)另一同学认为上述方案的实验步骤太繁琐,他认为,只要将样品溶于水后充分搅拌,加热蒸干灼烧称量即可,请你评价他的这个方案是否可行? 。(填“可行”或“不可行”)
 2Cu + SO2
2Cu + SO2