题目内容
16.将分别盛有熔融NaCl、MgCl2、Al2O3(熔有冰晶石)的三个电解槽,在一定条件下通电一段时间后,析出Na、Mg、Al的物质的量之比是( )| A. | 1:2:3 | B. | 3:2:1 | C. | 6:3:1 | D. | 6:3:2 |
分析 串联电路中电流强度相等,即通过的电子数相等,当通过1 mol电子时分别计算析出K、Mg、Al的物质的量,得到其物质的量之比.
解答 解:串联电路中电流强度相等,即通过的电子数相等,
由:KCl~1e-~K;MgCl2~2e-~Mg;Al2O3~6e-~2Al可知,
当通过1 mol电子时分别析出K、Mg、Al的物质的量为1、$\frac{1}{2}$、$\frac{1}{3}$,故其物质的量之比为1:$\frac{1}{2}$:$\frac{1}{3}$=6:3:2,
故选D.
点评 本题考查电解知识,题目难度不大,解答本题的关键是把握金属元素的化合价,能正确判断串联时析出金属物质的量的关系.

练习册系列答案
相关题目
6. 如图所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细,由此判断表中所列M、N、P物质,其中可以成立的是( )
如图所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细,由此判断表中所列M、N、P物质,其中可以成立的是( )
 如图所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细,由此判断表中所列M、N、P物质,其中可以成立的是( )
如图所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细,由此判断表中所列M、N、P物质,其中可以成立的是( ) | M | N | P | |
| A | Zn | Cu | 稀H2SO4溶液 |
| B | Cu | Fe | 稀HCl溶液 |
| C | Ag | Zn | AgNO3溶液 |
| D | Zn | Fe | Fe(NO3)3溶液 |
| A. | A | B. | B | C. | C | D. | D |
7.如图为碱性氢氧燃料电池原理示意图,按照此图的提示,下列叙述正确的是( )
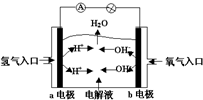

| A. | a电极是负极,电极反应为:H2-2e-═2H+ | |
| B. | b电极是正极,电极反应为:4OH-+4e-═2H2O+O2↑ | |
| C. | 电子从a极流向电流表、小灯泡、b极、通过电解质溶液形成闭合回路 | |
| D. | 电解质溶液中OH-向a极移动 |
4.下列水解的离子方程式正确的是( )
| A. | S2-+2H2O?H2S+2OH- | B. | CH3COO-+H2O?CH3COOH+OH- | ||
| C. | CH3COOH+H2O?CH3COO-+H3O+ | D. | Fe3++3H2O?Fe(OH)3↓+3H+ |
1.下列说法不正确的是( )
| A. | 在电解池中阴离子向阳极移动;在原电池中阴离子向正极移动 | |
| B. | 在电解池中,阳极发生氧化反应,在原电池中,负极发生氧化反应 | |
| C. | 电解池的阳极与电源的正极相连 | |
| D. | 电解过程中,电子从电源的负极流出到达阴极,从阳极流出回到电源的正极 |
8.已知C(s)+H2O(g)?CO(g)+H2(g)△H>0 达平衡后,下列条件有利于反应向正方向进行的是( )
| A. | 升高温度和减小压强 | B. | 降低温度和减小压强 | ||
| C. | 降低温度和增大压强 | D. | 升高温度和增大压强 |
5.如图为番茄电池,下列有关说法中不正确的是( )
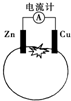

| A. | 一段时间后,锌片质量会变少 | B. | 铜电极附近会出现蓝色 | ||
| C. | 电流由铜通过导线流向锌 | D. | 锌电极是该电池的负极 |
6.X、Y是周期表前二十号元素,已知X、Y之间原子序数相差3,X、Y能形成化合物M.下列说法正确的是( )
| A. | 若X、Y处于同一周期,则化合物M不可能是正四面体型分子 | |
| B. | 若X的单质常温下是气体,则Y的单质常温下也是气体 | |
| C. | 若X、Y两元素周期数差1,则属于离子化合物的M只有四种 | |
| D. | 若M属于离子化合物,则其中可能含有非极性键 |