题目内容
8.已知C(s)+H2O(g)?CO(g)+H2(g)△H>0 达平衡后,下列条件有利于反应向正方向进行的是( )| A. | 升高温度和减小压强 | B. | 降低温度和减小压强 | ||
| C. | 降低温度和增大压强 | D. | 升高温度和增大压强 |
分析 根据升温时平衡正向移动,减小压强化学平衡向正反应方向移动来分析能使平衡向正反应方向移动的措施.
解答 解:对于反应A(g)+B(s)?2C(g)△H>0,反应是气体体积增大的吸热反应,升高温度和减小压强促进反应正向进行,
故选A.
点评 本题考查了化学平衡移动原理的应用,注意反应特征的分析判断,掌握基础是关键,题目较简单.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
18.下列烃的含氧衍生物中,只能与金属钠反应,不与碳酸氢钠溶液反应的是( )
| A. | CH2=CHCHO | B. | 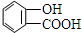 | C. | CH3COOCH3 | D. | 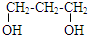 |
19.根据如表五种元素的第一至第四电离能数据(单位:kJ/mol),回答下面各题:
(1)在周期表中,最可能处于同一族的是E
A.Q和R B.S和T C.T和U D.R和T E.R和U
(2)下列离子的氧化性最弱的是D
A.S2+ B.R+ C.T3+ D.U+
(3)下列元素中,化学性质和物理性质最像Q元素的是C
A.硼 B.铍 C.氦 D.氢
(4)T元素最可能是p区元素,其氯化物的化学式为TCl3.
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
A.Q和R B.S和T C.T和U D.R和T E.R和U
(2)下列离子的氧化性最弱的是D
A.S2+ B.R+ C.T3+ D.U+
(3)下列元素中,化学性质和物理性质最像Q元素的是C
A.硼 B.铍 C.氦 D.氢
(4)T元素最可能是p区元素,其氯化物的化学式为TCl3.
16.将分别盛有熔融NaCl、MgCl2、Al2O3(熔有冰晶石)的三个电解槽,在一定条件下通电一段时间后,析出Na、Mg、Al的物质的量之比是( )
| A. | 1:2:3 | B. | 3:2:1 | C. | 6:3:1 | D. | 6:3:2 |
3.下列的判断或说法不正确的是( )
| A. | 溶解少量食盐于水中:△S>0 | |
| B. | 自发一定是放热反应 | |
| C. | 自发反应一定是熵增加或者放热反应 | |
| D. | CaCO3 (S) 分解成CaO (S) 和 CO2(g):△S>0 |
20.下列物质中,不属于电解质的是( )
| A. | 乙醇 | B. | CH3COOH | C. | BaCl2 | D. | Cl2 |
17.已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$的值与温度高低有关.当n(KOH)=a mol时,下列有关说法错误的是( )
| A. | 若某温度下,反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=11,则溶液中$\frac{c(Cl{O}^{-})}{c(Cl{{O}_{3}}^{-})}$=$\frac{1}{2}$ | |
| B. | 参加反应的氯气的物质的量等于$\frac{1}{2}$a mol | |
| C. | 改变温度,产物中KClO的最大理论产量为$\frac{1}{2}$a mol | |
| D. | 改变温度,产物中KClO3的最大理论产量为$\frac{1}{7}$a mol |
18.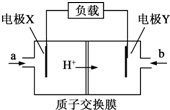 某氢氧燃料电池的原理如图所示.该电池的负极反应式为:H2-2e-═2H+.则下列判断中错误的是( )
某氢氧燃料电池的原理如图所示.该电池的负极反应式为:H2-2e-═2H+.则下列判断中错误的是( )
 某氢氧燃料电池的原理如图所示.该电池的负极反应式为:H2-2e-═2H+.则下列判断中错误的是( )
某氢氧燃料电池的原理如图所示.该电池的负极反应式为:H2-2e-═2H+.则下列判断中错误的是( )| A. | a处通入的是H2 | B. | 电解质溶液可能是NaOH溶液 | ||
| C. | 电极X是负极,被氧化 | D. | Y极的反应为O2+4e-+4H+═2H2O |