题目内容
5.如图为番茄电池,下列有关说法中不正确的是( )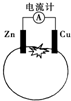
| A. | 一段时间后,锌片质量会变少 | B. | 铜电极附近会出现蓝色 | ||
| C. | 电流由铜通过导线流向锌 | D. | 锌电极是该电池的负极 |
分析 该装置为原电池,Zn易失电子作负极,Cu作正极,电子从负极沿导线流向正极,电流从正极流向负极,据此分析解答.
解答 解:A.锌作负极,锌失电子生成锌离子而逐渐被腐蚀,则锌的质量逐渐减少,故A正确;
B.该装置中Zn易失电子而作负极,Cu作正极,正极上番茄中的电解质溶液得电子发生还原反应,所以铜电极附近不会出现蓝色,故B错误;
C.锌作负极,铜作正极,电流从正极铜沿导线流向负极锌,故C正确;
D.锌易失电子发生氧化反应而作负极,故D正确;
故选B.
点评 本题以水果电池为载体考查了原电池原理,根据失电子的难易程度确定正负极,再结合电流的方向分析解答,难度不大.

练习册系列答案
相关题目
16.将分别盛有熔融NaCl、MgCl2、Al2O3(熔有冰晶石)的三个电解槽,在一定条件下通电一段时间后,析出Na、Mg、Al的物质的量之比是( )
| A. | 1:2:3 | B. | 3:2:1 | C. | 6:3:1 | D. | 6:3:2 |
20.下列物质中,不属于电解质的是( )
| A. | 乙醇 | B. | CH3COOH | C. | BaCl2 | D. | Cl2 |
10. 某同学组装了如图所示的电化学装置,电极ⅠAl,其它均为Cu,则下列正确的是( )
某同学组装了如图所示的电化学装置,电极ⅠAl,其它均为Cu,则下列正确的是( )
 某同学组装了如图所示的电化学装置,电极ⅠAl,其它均为Cu,则下列正确的是( )
某同学组装了如图所示的电化学装置,电极ⅠAl,其它均为Cu,则下列正确的是( )| A. | 电流方向:电极Ⅳ→A→电极Ⅰ | B. | 电极Ⅰ发生还原反应 | ||
| C. | 电极Ⅱ逐渐溶解 | D. | 电极Ⅲ的电极反应:Cu2++2e-=Cu |
17.已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$的值与温度高低有关.当n(KOH)=a mol时,下列有关说法错误的是( )
| A. | 若某温度下,反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=11,则溶液中$\frac{c(Cl{O}^{-})}{c(Cl{{O}_{3}}^{-})}$=$\frac{1}{2}$ | |
| B. | 参加反应的氯气的物质的量等于$\frac{1}{2}$a mol | |
| C. | 改变温度,产物中KClO的最大理论产量为$\frac{1}{2}$a mol | |
| D. | 改变温度,产物中KClO3的最大理论产量为$\frac{1}{7}$a mol |

 ;
; 研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.
研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.