题目内容
14.下列关于NA的说法中,不正确的是( )| A. | 2NA个H2与NA个O2的质量比为1:8 | |
| B. | 0.5NA个HCl所占的体积约为11.2L | |
| C. | 71gCl2所含的Cl数目为2NA | |
| D. | 1L 0.5mol•L-1FeCl3溶液中含有1.5NA个Cl- |
分析 A.依据m=$\frac{N}{{N}_{A}}$×M计算解答;
B.气体状况未知,气体摩尔体积未知;
C.71g Cl2的物质的量为1mol,含有2mol氯原子;
D.0.5mol•L-1FeCl3溶液中,氯离子浓度为1.5mol/L,依据n=cv计算.
解答 解:A.2NA个H2的质量为:$\frac{2{N}_{A}}{{N}_{A}}$×2g/mol=4g,NA个O2的质量为1mol×32g/mol=32g,二者质量之比为1:8,故A正确;
B.气体状况未知,气体摩尔体积未知,无法计算,故B错误;
C.71g Cl2的物质的量为1mol,含有2mol氯原子,个数为2NA,故C正确;
D.0.5mol•L-1FeCl3溶液中,氯离子浓度为1.5mol/L,1L 0.5mol•L-1FeCl3溶液中含有Cl-1.5mol/L×1L×NA=1.5NA个,故D正确;
故选:B.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,明确标况下气体摩尔体积的使用条件,题目难度不大.

练习册系列答案
相关题目
4.等体积、等浓度的浓硫酸分别与足量的炭粉、铜粉在一定条件下完全反应.下列指定“物理量”之比不是2:1的是( )
| A. | 转移电子的物质的量 | B. | 产生SO2的物质的量 | ||
| C. | 氧化剂的物质的量 | D. | 生成水的物质的量 |
19.实验室中需要配制2mol/L的NaOH溶液850mL,配制时应选用的容量瓶的规格和称取的NaOH的质量分别是( )
| A. | 950mL,76g | B. | 500mL,80g | C. | 1000mL,80g | D. | 1000mL,76g |
10. 天然维生素P(结构如图,分子结构中R为饱和烃基)存在于槐树花蕾中,它是一种营养增补剂,关于维生素P的叙述正确的是( )
天然维生素P(结构如图,分子结构中R为饱和烃基)存在于槐树花蕾中,它是一种营养增补剂,关于维生素P的叙述正确的是( )
 天然维生素P(结构如图,分子结构中R为饱和烃基)存在于槐树花蕾中,它是一种营养增补剂,关于维生素P的叙述正确的是( )
天然维生素P(结构如图,分子结构中R为饱和烃基)存在于槐树花蕾中,它是一种营养增补剂,关于维生素P的叙述正确的是( )| A. | 可与溴水反应,且1 mol该物质与足量溴水反应消耗6 mol Br2 | |
| B. | 可与NaOH溶液反应,1 mol该物质可与5 mol NaOH反应 | |
| C. | 一定条件下1 mol该物质可与H2加成,耗H2最大量为6 mol | |
| D. | 维生素P能发生水解反应 |
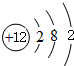 ;画出BC2的电子式
;画出BC2的电子式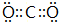 ,结构式O=C=O,其晶体类型为分子晶体
,结构式O=C=O,其晶体类型为分子晶体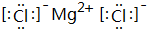 ,其晶体类型为离子晶体.
,其晶体类型为离子晶体.