题目内容
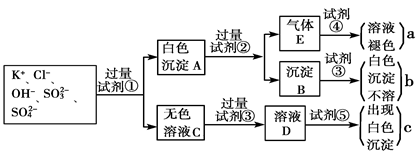
(8分)有一瓶澄清的溶液,其中可能含有NH4+、K+、 Ba2+、Al3+、Fe3+、 I-、NO3-、CO32-、SO42-、AlO2- 。取该溶液进行以下实验:
①用pH试纸检验,溶液呈强酸性。
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色。
③另取溶液适量,逐滴加入NaOH溶液:a.溶液从酸性变为中性;b.溶液逐渐产生沉淀;c.沉淀完全溶解;d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
④取适量③得到的碱性溶液加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)由①可以排除 离子的存在。
(2)由②可以证明 离子的存在,同时排除 离子存在。理由是_________________________。
(3)由③可证明 离子存在。
(4)由④可以排除 离子存在,同时证明 离子的存在。
(1)CO32 -、AlO2-;
(2)I-;Fe3+、NO3-;因为CCl4层呈现出碘的颜色;Fe3+、NO3-在该环境中与I-不能共存。
(3)Al3+、NH4+;(4)SO42-;Ba2+。
解析试题分析:(1)①用pH试纸检验,溶液呈强酸性,则由于CO32-、AlO2- 与H+会发生离子而不能大量共存,因此CO32 -、AlO2-不能大量存在;(2)②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色证明在溶液中含有I-。由于I-、与Fe3+、NO3-、在酸性环境会发生氧化还原反应而不能大量存在,因此在证明I-存在的同时排除Fe3+、NO3-的存在;(3)③另取溶液适量,逐滴加入NaOH溶液:a.溶液从酸性变为中性;b.溶液逐渐产生沉淀;c.沉淀完全溶解; d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。证明含有Al3+、NH4+;(4)④取适量③得到的碱性溶液加入Na2CO3溶液,有白色沉淀生成。则证明在原溶液中含有Ba2+,由于SO42-在酸性环境也会形成沉淀,因此就可以排除SO42-离子的存在。
考点:考查离子的检验、离子共存的知识。

 小学能力测试卷系列答案
小学能力测试卷系列答案下列反应的离子方程式正确的是
| A.向稀氨水中加入稀盐酸 OH- + H+ =H2O |
| B.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ |
| C.碳酸钙溶于醋酸中 CaCO3 + 2H+ =Ca2+ + H2O + CO2↑ |
| D.碳酸氢钙溶液跟稀硝酸反应 HCO3-+ H+ = H2O + CO2↑ |
若溶液中由水电离产生的C (OH-)=1×10-14mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是:
| A.Al3+ Na+NO3- Cl- | B.K+ Na+Cl- NO3- |
| C.K+ Na+ Cl-AlO2- | D.K+ NH4+ SO42-NO3- |
(14分)Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第 周期第 族;S的基态原子核外有 个未成对电子;Si的基态原子核外电子排布式为 。
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si S | O2- Na+ | NaCl Si | H2SO4 HClO4 |
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101KPa下,已知该反应每消耗1 mol CuCl2(s),放热44.4KJ,该反应的热化学方程式是 。
(4)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目 。
(10分)某科研小组设计出利用工业废酸(l0%)来堆浸某废弃的氧化铜锌矿的方案,实现废物综合利用,如下图所示。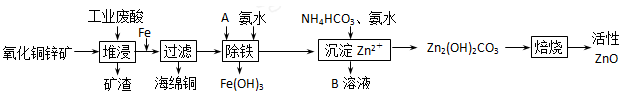
已知:各离子开始沉淀及完全沉淀时的pH如下表所示。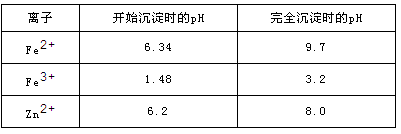
请回答下列问题:
(1)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS
不溶,则相同温度下:Ksp(CuS)______Ksp(ZnS)(选填“>”“<”或“=”)。
(2)物质A可使用下列物质中的 。
| A.KMnO4 | B.O2 | C.H2O2 | D.Cl2 |
(4)物质B可直接用作氮肥,则B的化学式是________。
(5)除铁后得到的Fe(OH)3可用KClO溶液在碱性环境下将其氧化得到一种高效的多功能水处理剂——K2FeO4,写出该反应的离子方程式__________。

 2Fe(s)+3CO(g)△H=+489.0KJ·mol
2Fe(s)+3CO(g)△H=+489.0KJ·mol ;
;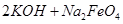 =
=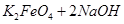 ,说明此温度下
,说明此温度下 __________
__________ 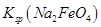 (填“>”或“<”)。
(填“>”或“<”)。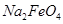 完全转化为
完全转化为 ,若最终制得粗产品
,若最终制得粗产品 3Zn(OH)2+2Fe(OH)3+4KOH,放电时电池的负极反应式为______________________________________。
3Zn(OH)2+2Fe(OH)3+4KOH,放电时电池的负极反应式为______________________________________。