题目内容
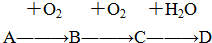 A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如图所示(反应条件及其他物质已经略去):
A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如图所示(反应条件及其他物质已经略去):请回答下列问题:
(1)若常温下A为淡黄色固体单质,D为强酸,则写出D→B的化学方程式:
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使湿润的蓝色石蕊试纸变红.则A为
考点:无机物的推断
专题:推断题
分析:A、B、C、D均为中学所学的常见物质且均含有同一种元素,
(1)若常温下A为淡黄色固体单质,D为强酸,则A是S,根据转化关系知,B是SO2、C是SO3、D是H2SO4,浓硫酸和铜在加热条件下能生成二氧化硫;
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,则A是NH3,D的稀溶液能使湿润的蓝色石蕊试纸变红,为酸,氨气被氧化生成NO,NO被氧气氧化生成NO2,所以B是NO、C是NO2、D是HNO3,在加热催化剂条件下、氨气被氧化生成NO和水.
(1)若常温下A为淡黄色固体单质,D为强酸,则A是S,根据转化关系知,B是SO2、C是SO3、D是H2SO4,浓硫酸和铜在加热条件下能生成二氧化硫;
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,则A是NH3,D的稀溶液能使湿润的蓝色石蕊试纸变红,为酸,氨气被氧化生成NO,NO被氧气氧化生成NO2,所以B是NO、C是NO2、D是HNO3,在加热催化剂条件下、氨气被氧化生成NO和水.
解答:
解:(1)若常温下A为淡黄色固体单质,D为强酸,则A是S,根据转化关系知,B是SO2、C是SO3、D是H2SO4,浓硫酸和铜在加热条件下能生成二氧化硫,反应方程式为Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,则A是NH3,D的稀溶液能使湿润的蓝色石蕊试纸变红,为酸,氨气被氧化生成NO,NO被氧气氧化生成NO2,所以B是NO、C是NO2、D是HNO3,在加热催化剂条件下、氨气被氧化生成NO和水,反应方程式为4NH3+5O2
4NO+6H2O,故答案为:NH3;4NH3+5O2
4NO+6H2O.
| ||
| ||
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,则A是NH3,D的稀溶液能使湿润的蓝色石蕊试纸变红,为酸,氨气被氧化生成NO,NO被氧气氧化生成NO2,所以B是NO、C是NO2、D是HNO3,在加热催化剂条件下、氨气被氧化生成NO和水,反应方程式为4NH3+5O2
| ||
| △ |
| ||
| △ |
点评:本题考查了无机物推断,根据物质的颜色、物质的性质进行推断,A能连续被氧化,说明A中存在的某种元素有多种化合价,再结合D的性质分析解答,题目难度不大.

练习册系列答案
相关题目
在体积恒定的密闭容器中,一定量的SO2与1mol O2在催化剂作用下加热到600℃发生反应:2SO2+O2
2SO3△H<0.当气体的物质的量减少0.5mol时反应达到平衡.下列叙述正确的是( )
| 催化剂 |
| 加热 |
| A、当SO3的生成速率与SO2的消耗速率相等时反应达到平衡 |
| B、降低温度,正反应速率减小程度比逆反应速率减小程度大 |
| C、将平衡混合气体通入过量BaCl2溶液中,会得到两种白色沉淀 |
| D、该反应过程中转移了2mol电子 |
意大利科学家最近合成了一种新型的氧分子,其化学式为O4,对其说法正确的是( )
| A、O4是一种化合物 |
| B、O4是由O2组成的混合物 |
| C、O4是一种单质 |
| D、一个O4分子由2个O2分子构成 |
下列说法不正确的是( )
| A、长期使用阿司匹林会出现水杨酸中毒表现,应立即停药,静脉注射碳酸氢钠溶液 |
| B、红宝石、水晶、钻石的主要成分都是硅酸盐 |
| C、高温条件下可杀死H7N9型禽流感病毒,属于蛋白质的变性 |
| D、石油裂解、煤的气化、海水制镁都包含化学变化 |
 请认真观察图,然后回答问题.
请认真观察图,然后回答问题.