题目内容
某些化学反应可表示为:A+B→C+D+H2O.请回答下列问题:
(1)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,则该反应离子方程式为 .
(2)若A为黑色固体,C是黄绿色气体,则该反应的化学方程式为 .
(3)若C为NaCl,D是能使澄清石灰水变浑浊的无色无味的气体,若A为盐,B为酸,则A是 或 (填化学式).
(4)若A是铁的一种氧化物,B是盐酸,则A与B反应的化学方程式为 .
(1)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,则该反应离子方程式为
(2)若A为黑色固体,C是黄绿色气体,则该反应的化学方程式为
(3)若C为NaCl,D是能使澄清石灰水变浑浊的无色无味的气体,若A为盐,B为酸,则A是
(4)若A是铁的一种氧化物,B是盐酸,则A与B反应的化学方程式为
考点:无机物的推断
专题:推断题
分析:(1)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,则该反应为氯气和强碱的反应;
(2)若A为黑色固体,C是黄绿色气体,则C是氯气、A是二氧化锰,该反应是浓盐酸和二氧化锰制取氯气的反应;
(3)若C为NaCl,D是能使澄清石灰水变浑浊的无色无味的气体,为二氧化碳,若A为盐,B为酸,则A是 碳酸钠或碳酸氢钠;
(4)若A是铁的一种氧化物,B是盐酸,能和盐酸生成两种盐的铁的氧化物为四氧化三铁.
(2)若A为黑色固体,C是黄绿色气体,则C是氯气、A是二氧化锰,该反应是浓盐酸和二氧化锰制取氯气的反应;
(3)若C为NaCl,D是能使澄清石灰水变浑浊的无色无味的气体,为二氧化碳,若A为盐,B为酸,则A是 碳酸钠或碳酸氢钠;
(4)若A是铁的一种氧化物,B是盐酸,能和盐酸生成两种盐的铁的氧化物为四氧化三铁.
解答:
解:(1)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,则该反应为氯气和强碱的反应,离子方程式为Cl2+2OH-═Cl-+ClO-+H2O 或 3Cl2+6OH -═5Cl-+ClO3-+3H2O,故答案为:Cl2+2OH-═Cl-+ClO-+H2O 或 3Cl2+6OH -═5Cl-+ClO3-+3H2O;
(2)若A为黑色固体,C是黄绿色气体,则C是氯气、A是二氧化锰,该反应是浓盐酸和二氧化锰制取氯气的反应,二者反应生成氯化锰、氯气和水,反应方程式为MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
(3)若C为NaCl,D是能使澄清石灰水变浑浊的无色无味的气体,为二氧化碳,若A为盐,B为酸,能和酸反应生成二氧化碳的物质为碳酸盐或碳酸氢盐,再结合钠原子守恒知,A是Na2CO3或NaHCO3,
故答案为:Na2CO3;NaHCO3;
(4)若A是铁的一种氧化物,B是盐酸,能和盐酸生成两种盐的铁的氧化物为四氧化三铁,二者反应生成氯化铁、氯化亚铁和水,反应方程式为Fe3O4+8HCl═FeCl2+2FeCl3+4H2O,故答案为:Fe3O4+8HCl═FeCl2+2FeCl3+4H2O.
(2)若A为黑色固体,C是黄绿色气体,则C是氯气、A是二氧化锰,该反应是浓盐酸和二氧化锰制取氯气的反应,二者反应生成氯化锰、氯气和水,反应方程式为MnO2+4HCl(浓)
| ||
| ||
(3)若C为NaCl,D是能使澄清石灰水变浑浊的无色无味的气体,为二氧化碳,若A为盐,B为酸,能和酸反应生成二氧化碳的物质为碳酸盐或碳酸氢盐,再结合钠原子守恒知,A是Na2CO3或NaHCO3,
故答案为:Na2CO3;NaHCO3;
(4)若A是铁的一种氧化物,B是盐酸,能和盐酸生成两种盐的铁的氧化物为四氧化三铁,二者反应生成氯化铁、氯化亚铁和水,反应方程式为Fe3O4+8HCl═FeCl2+2FeCl3+4H2O,故答案为:Fe3O4+8HCl═FeCl2+2FeCl3+4H2O.
点评:本题考查了无机物推断,涉及铁、氯气、钠的化合物等知识点的考查,同时考查学生对元素化合物知识的掌握,根据物质的性质及反应特点分析解答,题目难度中等.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
氢气是人类最理想的能源.已知在25℃、101kPa下,1g氢气完全燃烧生成液态水时放出热量142.9kJ,则下列热化学方程式书写正确的是( )
| A、2H2+O2═2H2O;△H=-142.9kJ/mol |
| B、2H2(g)+O2(g)═2H2O(l);△H=-142.9kJ/mol |
| C、2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ/mol |
| D、2H2(g)+O2(g)═2H2O(l);△H=+571.6kJ/mol |
在MgCl2和AlCl3的混合液中,Cl-的物质的量为0.7mol.向该溶液中加入100mL 8mol/L的KOH溶液,使之充分反应.若反应前Al3+的物质的量与混合溶液中离子总物质的量的比值为x.以下说法正确的是( )
A、若反应前Al3+的物质的量为a mol,则a=
| ||
| B、只有当x为0.1时,加入87.5mL的KOH,溶液中的阳离子恰好完全沉淀 | ||
| C、当100mL KOH刚好完全消耗,且Al3+全部转化为AlO2-时,x的值为0.2 | ||
| D、x的取值范围是0<x≤0.25 |

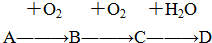 A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如图所示(反应条件及其他物质已经略去):
A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如图所示(反应条件及其他物质已经略去):