题目内容
(1)AlCl3的水溶液常温时的pH 7(填“>”、“=”、“<”),实验室在配制AlCl3溶液时,常将AlCl3固体先溶于水中,然后滴加少量稀盐酸,其作用是 .
(2)醋酸钠(NaAc)水溶液呈 性,原因是 (用离子方程式表示).
(2)醋酸钠(NaAc)水溶液呈
考点:盐类水解的应用
专题:盐类的水解专题
分析:(1)AlCl3是强酸弱碱盐水解成酸性,加酸是为了抑制Al3+的水解;
(2)CH3COO-是弱酸的阴离子,能水解 CH3COO-+H2O?CH3COOH+OH-溶液呈碱性.
(2)CH3COO-是弱酸的阴离子,能水解 CH3COO-+H2O?CH3COOH+OH-溶液呈碱性.
解答:
解:(1)AlCl3是强酸弱碱盐水解成酸性,加酸是为了抑制Al3+的水解,故答案为:<;抑制Al3+的水解.
(2)CH3COO-是弱酸的阴离子,能水解 CH3COO-+H2O?CH3COOH+OH-溶液呈碱性,故答案为:碱性;CH3COO-+H2O?CH3COOH+OH-.
(2)CH3COO-是弱酸的阴离子,能水解 CH3COO-+H2O?CH3COOH+OH-溶液呈碱性,故答案为:碱性;CH3COO-+H2O?CH3COOH+OH-.
点评:本题考查了盐类水解的有关知识,注意影响水解平衡的因素,题目比较基础.

练习册系列答案
相关题目
下列说法正确的是( )
| A、氮原子的质量就是氮的相对原子质量 |
| B、氢氧化钠的摩尔质量是40g |
| C、氩气的摩尔质量在数值上等于它的相对原子质量 |
| D、1mol H2SO4中含有1mol H2 |
如果25℃时KW=10-14,100℃时KW=10-12,这说明( )
| A、100℃时水的电离常数较大 |
| B、前者c(H+)比后者大 |
| C、水的电离过程是一个放热过程 |
| D、KW和K电离无直接关系 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、在反应KIO3+6HI═KI+3I2+3H2O中,每生成3mol I2转移的电子数为5NA |
| B、100mL 18.4mol?L-1硫酸与足量Cu反应,生成SO2的分子数为0.92NA |
| C、1L 0.1mol?L-1的CH3COOH溶液中所含的离子和分子总数为0.1NA |
| D、将0.1mol FeCl3滴入沸水中可制得0.1NA Fe(OH)3胶粒 |
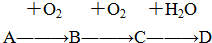 A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如图所示(反应条件及其他物质已经略去):
A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如图所示(反应条件及其他物质已经略去):