题目内容
【题目】Ⅰ.已知C、H2、CO的燃烧热的数据如表所示:
物质 | C | H2 | CO |
ΔH/kJ·mol-1 | -393.5 | -285.8 | -283.0 |
(1)写出C完全燃烧的热化学方程式:_____。
(2)能表示H2燃烧热的热化学方程式为____。
(3)现以H2或CO为燃料来提供热能,从热能的角度考虑,你认为最好选择__(填写序号)。
A.H2 B.CO C.均可以
理由是___。
Ⅱ.已知下列热化学方程式:
①H2O(l)=H2(g)+![]() O2(g) ΔH=+285.8 kJ/mol
O2(g) ΔH=+285.8 kJ/mol
②H2(g)+![]() O2(g)=H2O(g) ΔH=-241.8 kJ/mol
O2(g)=H2O(g) ΔH=-241.8 kJ/mol
③NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3 kJ/mol
回答下列问题:
(4)上述反应中属于吸热反应的是___(填序号)。
(5)燃烧10gH2生成液态水,放出的热量为___。
【答案】C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8kJ/mol A 等质量的H2完全燃烧放出的热量比CO多,且H2的燃烧产物为H2O,对环境无污染 ① 1429 kJ
O2(g)=H2O(l) ΔH=-285.8kJ/mol A 等质量的H2完全燃烧放出的热量比CO多,且H2的燃烧产物为H2O,对环境无污染 ① 1429 kJ
【解析】
⑴C完全燃烧的热化学方程式为C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol,
⑵H2燃烧热的热化学方程式为H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8kJ/mol,
O2(g)=H2O(l) ΔH=-285.8kJ/mol,
⑶H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8kJ/mol,
O2(g)=H2O(l) ΔH=-285.8kJ/mol,
CO(g)+![]() O2(g)=CO2(g) ΔH=--283.0 kJ/mol,等质量的H2完全燃烧放出的热量比CO多,且H2的燃烧产物为H2O,对环境无污染,因此从热能的角度考虑,H2为燃料来提供热能是最好选择,故答案为A;等质量的H2完全燃烧放出的热量比CO多,且H2的燃烧产物为H2O,对环境无污染
O2(g)=CO2(g) ΔH=--283.0 kJ/mol,等质量的H2完全燃烧放出的热量比CO多,且H2的燃烧产物为H2O,对环境无污染,因此从热能的角度考虑,H2为燃料来提供热能是最好选择,故答案为A;等质量的H2完全燃烧放出的热量比CO多,且H2的燃烧产物为H2O,对环境无污染
⑷①H2O(l)=H2(g)+![]() O2(g) ΔH=+285.8 kJ/mol是吸热反应,
O2(g) ΔH=+285.8 kJ/mol是吸热反应,
②H2(g)+![]() O2(g)=H2O(g) ΔH=-241.8 kJ/mol是放热反应,
O2(g)=H2O(g) ΔH=-241.8 kJ/mol是放热反应,
③NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3 kJ/mol是放热反应,
故答案为①;
氢气燃烧热的热化学方程式为H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8kJ/mol,
O2(g)=H2O(l) ΔH=-285.8kJ/mol,
10g氢气物质的量为![]() ,放出的热量Q=285.8kJ/mol×5mol = 1429 kJ,故答案为1429 kJ。
,放出的热量Q=285.8kJ/mol×5mol = 1429 kJ,故答案为1429 kJ。

【题目】经测定乙醇的分子式为C2H6O。由于有机物普遍存在同分异构现象,推测乙醇结构可能是下列两种之一:(I)CH3CH2OH(II)CH3OCH3。为测定其结构,应利用物质的特殊性进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,请甲、乙、丙三位同学直接利用如图给定的装置进行实验,确定乙醇的结构。
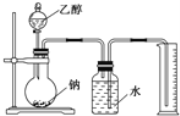
(1)学生甲得到一组实验数据:
乙醇的物质的量(mol) | 氢气的体积(标况)(L) |
0.10 | 1.13 |
0.10 | 1.11 |
0.10 | 1.12 |
0.10 | 1.18 |
请根据上表,帮助甲同学正确处理实验数据,氢气体积的平均值为__(L),由此推断乙醇的结构应为__式(用I或II表示),理由是___。写出乙醇与钠反应的化学方程式:___。
(2)同学乙分别准确称量4.60g乙醇进行多次实验,结果发现以排到量筒内的水的体积,作为生成的H2体积总是小于1.12L(换算成标准状况后)。如果忽略量筒本身及读数造成的误差,那么乙认为可能是由于样品中含有少量水造成的,你认为正确吗?___(填“正确”或“不正确”)。如果不正确,请说明理由:____。
(3)同学丙认为实验成功的关键有:①装置气密性要良好②实验开始前准确确定乙醇的量③钠足量④广口瓶内必须有足量水⑤氢气体积的测算方法正确、数值准确⑥应了解实验时的温度和大气压强。其中正确的有____。(填序号)