题目内容
16.按要求回答下列问题:(1)
 的名称为3,3,6-三甲基辛烷;
的名称为3,3,6-三甲基辛烷;(2)
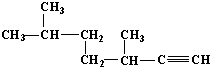 的名称为3,6-二甲基-1-庚炔;
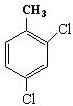
的名称为3,6-二甲基-1-庚炔;(3)2,4-二氯甲苯的结构简式为
 ;
;(4)某物质结构如图所示
 ,分子式为C15H22O2;
,分子式为C15H22O2; 该物质可以与下列ABCD(填序号)发生反应.
A.KMnO4酸性溶液 B.氢气 C.溴水 D.NaOH溶液
(5)
 中含有的官能团的名称为羟基,酯基.
中含有的官能团的名称为羟基,酯基.
分析 (1)该有机物为烷烃,选取最长碳链为主链,然后从取代基编号之和最长的一端编号,先写出取代基位置,在写出主链名称;
(2)该有机物为炔烃,选取含有碳碳三键的最长碳链为主链,然后从距离碳碳三键最近的一端开始编号,命名中需要标出碳碳三键的位置;
(3)甲基连接的碳为1号C,在2、4号C各含有应该氯原子;
(4)根据图示的有机物结构简式写出分子式;根据该有机物结构判断具有的化学性质;
(5)根据结构简式 可知,该有机物分子中含有的官能团为羟基和酯基.
可知,该有机物分子中含有的官能团为羟基和酯基.
解答 解:(1) ,该有机物分子中最长碳链含有8个C,主链为辛烷,从右上方开始编号,在3号C含有2个甲基、在6号C含有1个甲基,该有机物名称为:3,3,6-三甲基辛烷,故答案为:3,3,6-三甲基辛烷;
,该有机物分子中最长碳链含有8个C,主链为辛烷,从右上方开始编号,在3号C含有2个甲基、在6号C含有1个甲基,该有机物名称为:3,3,6-三甲基辛烷,故答案为:3,3,6-三甲基辛烷;
(2)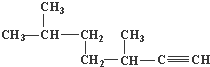 ,该有机物为炔烃,选取含有碳碳三键的最长碳链为主链,该有机物最长碳链含有7个C,主链为庚炔,编号从右边开始,碳碳三键在1号C,在3、6号C各含有1个甲基,该有机物名称为:3,6-二甲基-1-庚炔,故答案为:3,6-二甲基-1-庚炔;
,该有机物为炔烃,选取含有碳碳三键的最长碳链为主链,该有机物最长碳链含有7个C,主链为庚炔,编号从右边开始,碳碳三键在1号C,在3、6号C各含有1个甲基,该有机物名称为:3,6-二甲基-1-庚炔,故答案为:3,6-二甲基-1-庚炔;
(3)2,4-二氯甲苯的主链为甲苯,甲苯所在的C为1号C,在2、4号C各含有一个氯原子,该有机物结构简式为 ,故答案为:
,故答案为: ;
;
(4)该有机物分子中含有15个C、22个H和2个O,该有机物的分子式为:C15H22O2;该有机物含有碳碳双键,能够与被酸性高锰酸钾溶液氧化,能够与氢气发生加成反应,能够使溴水褪色;分子中还含有羧基,能够与氢氧化钠溶液发生中和反应,所以ABCD都正确,故答案为:C15H22O2;ABCD;
(5) 中含有的官能团为羟基、酯基,故答案为:羟基;酯基.
中含有的官能团为羟基、酯基,故答案为:羟基;酯基.
点评 本题考查了有机物结构与性质,题目难度中等,试题涉及的题量较大,知识点较多,充分考查了学生对所学知识的掌握情况,注意掌握常见有机物结构与性质,明确有机物命名原则,能够正确书写常见有机物的结构简式.

 名校课堂系列答案
名校课堂系列答案(A)NaOH+HCl=NaCl+H2O
(B)2FeCl3+Cu=2FeCl2+CuCl2
①根据两反应本质,判断能设计成原电池的反应是B(填序号).
(2)选择适宜的材料和试剂将(1)中你的选择设计为一个原电池.
①在图1的方框中画出装置图并说明电解质溶液.②写出电极反应式.
| 电极 | 电极材料 | 电极反应式 |
| 负极 | ||
| 正极 |
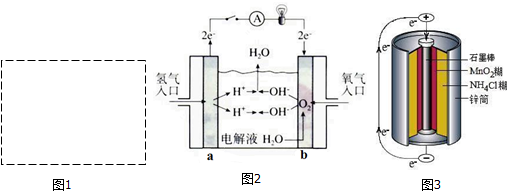
①该燃料电池的负极是a(写a或b).
②O2 (写化学式)发生还原反应.
③燃料电池中是将化学能转化为电能,总反应式是2H2+O2=2H2O.
(4)锌锰干电池是最早使用的化学电池,其基本构造如图3所示.锌锰干电池的负极是锌,电路中每通过0.4mole-,负极质量减少13g;工作时NH4+离子在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是2NH4++2e-=2NH3↑+H2↑.
| R | ||
| X | Y | Z |
| A. | Y的氢化物比Z的氢化物稳定 | |
| B. | 原子半径大小顺序是X>Y>R | |
| C. | Y、R形成的化台物YR3能使酸性KMnO4溶液褪色 | |
| D. | 四种元素中最高价氧化物的水化物的酸性最强的是Y |
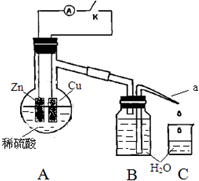 某同学分析Zn与稀H2SO4的反应.
某同学分析Zn与稀H2SO4的反应.(1)该反应的离子方程式是Zn+2H+=Zn2++H2↑.
(2)制H2时,用稀硫酸而不用浓硫酸,原因是浓H2SO4具有强氧化性,不能生成氢气.
(3)已知:Zn(s)+$\frac{1}{2}$O2(g)=ZnO(s)△H=-332kJ/mol
ZnO(s)+H2SO4(aq)=ZnSO4(aq)+H2O(l)△H=-112kJ/mol
H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-286kJ/mol
则Zn与稀H2SO4反应生成1mol H2 时的反应热△H=-158kJ/mol.
(4)该同学用如下装置进行实验,分析影响反应速率的因素.
实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1 分钟内从a管流出的水滴数,得到的水滴数如下表所示:
| 1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
| 1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
①由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率快(填“快”或“慢”),主要原因是形成原电池反应速度快.
②由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是断开K时,溶液中的c(H+)大于闭合K时溶液中的c(H+).
③从能量转换形式不同的角度,分析水滴数86>81、117>112的主要原因是断开K时,反应的化学能主要转化成热能,闭合K时,反应的化学能主要转化成电能,前者使溶液的温度升得更高,故反应速率更快.
| A. | 决定反应速率的因素只有催化剂 | |
| B. | 食物放在冰箱中会减慢食物变质的速率 | |
| C. | 锌与稀硫酸反应时,加入少量水能加快产生氢气的速率 | |
| D. | 增大压强一定能使化学反应速率加快 |
| A. | 三种 | B. | 四种 | C. | 五种 | D. | 六种 |
| A. | 原子半径:Na>Mg>O | |
| B. | 13C和14C属于同位素 | |
| C. | 0族元素是同周期中非金属性最强的元素 | |
| D. | N和P属于第ⅤA族元素,HNO3酸性比H3PO4的强 |
| A. | 1mol | B. | 1.5mol | C. | 2mol | D. | 3mol |