题目内容
6.向含有1mol配合物[Co(NH3)5Cl]Cl2的溶液中加入足量的硝酸银溶液,得到的沉淀物质的量为( )| A. | 1mol | B. | 1.5mol | C. | 2mol | D. | 3mol |
分析 配合物也叫络合物,为一类具有特征化学结构的化合物,由中心原子或离子(统称中心原子)和围绕它的称为配位体(简称配体)的分子或离子,完全或部分由配位键结合形成.在配合物[Co(NH3)5Cl]Cl2中,有一个氯离子中内界,有两个氯离子在外界,溶液中能与银离子反应生成沉淀的是在外界的氯离子,由此可推断生成氯化银沉淀的物质的量.
解答 解:在配合物[Co(NH3)5Cl]Cl2中,外界是Cl-,內界是[Co(NH3)5Cl]2+,有一个氯离子中内界,有两个氯离子在外界,[Co(NH3)5Cl]Cl2的电离方程式为[Co(NH3)5Cl]Cl2=[Co(NH3)5Cl]2++2Cl-,溶液中能与银离子反应生成沉淀的是在外界的氯离子,所以依据Ag++Cl-=AgCl↓可知,1mol此配合物电离产生2mol氯离子,由此可推断1mol配合物[Co(NH3)5Cl]Cl2的溶液中加入足量的AgNO3溶液,生成氯化银沉的物质的量是2mol,
故选C.
点评 本题主要考查了配合物的性质,明确配合物的外界能产生自由移动的离子,但內界不产生自由移动的离子是解题的关键,注意配体、中心离子、外界离子以及配位数的判断,题目难度中等.

练习册系列答案
相关题目
14.阿斯匹林的结构简式为: 则1mol阿斯匹林跟足量氢氧化钠溶液充分反应,消耗氢氧化钠的物质的量为( )
则1mol阿斯匹林跟足量氢氧化钠溶液充分反应,消耗氢氧化钠的物质的量为( )
 则1mol阿斯匹林跟足量氢氧化钠溶液充分反应,消耗氢氧化钠的物质的量为( )
则1mol阿斯匹林跟足量氢氧化钠溶液充分反应,消耗氢氧化钠的物质的量为( )| A. | 1mol | B. | 2mol | C. | 3mol | D. | 4mol |
1.化合物HIn在水溶液中因存在以下电离平衡:HIn(aq,红色)?H++In-(aq,黄色),故可用作酸碱指示剂.浓度为0.02mol/L的下列各溶液:(1)HCl (2)石灰水 (3)NaCl(aq) (4)NaHCO3(aq),其中能使指示剂显红色的是( )
| A. | (1) | B. | (2) | C. | (3) | D. | (4) |
11.下列各组数值表示有关元素的原子序数,其所表示的各原子中,能以离子键相互结合成AB2型稳定化合物的是( )
| A. | 18和12 | B. | 6和8 | C. | 11和16 | D. | 12和9 |
18.下列气体无色无味的是( )
| A. | 氯气 | B. | 二氧化硫 | C. | 氨气 | D. | 氮气 |
16.可逆反应aA(s)+bB(g)?cC(g)+dD(g),反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示,据图分析,以下正确的是( )
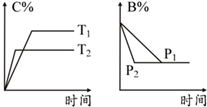

| A. | T1>T2 | B. | 正反应为放热反应 | ||
| C. | P1>P2 | D. | a+b=c+d |
 的名称为3,3,6-三甲基辛烷;
的名称为3,3,6-三甲基辛烷; 的名称为3,6-二甲基-1-庚炔;
的名称为3,6-二甲基-1-庚炔; ;
; ,分子式为C15H22O2;
,分子式为C15H22O2;  中含有的官能团的名称为羟基,酯基.
中含有的官能团的名称为羟基,酯基. .
. ,反应类型取代反应.
,反应类型取代反应.