题目内容
4.如图为短周期的一部分,Y原子最外层电子数是其电子层数的2倍,下列说法正确的是(| R | ||
| X | Y | Z |
| A. | Y的氢化物比Z的氢化物稳定 | |
| B. | 原子半径大小顺序是X>Y>R | |
| C. | Y、R形成的化台物YR3能使酸性KMnO4溶液褪色 | |
| D. | 四种元素中最高价氧化物的水化物的酸性最强的是Y |
分析 X、Y、R、Z为短周期元素,由元素在周期表中的位置可知,R处于第二周期,X、Y、Z处于第三周期,Y原子最外层电子数是其电子层数的2倍,故最外层电子数为6,则Y为S元素,则X为P元素、Z为Cl元素、R为O元素,结合元素周期律知识解答该题.
解答 解:X、Y、R、Z为短周期元素,由元素在周期表中的位置可知,R处于第二周期,X、Y、Z处于第三周期,Y原子最外层电子数是其电子层数的2倍,故最外层电子数为6,则Y为S元素,则X为P元素、Z为Cl元素、R为O元素,
A、同周期元素从左到右元素的非金属性逐渐增强,故非金属性Z>Y,非金属性越强,氢化物越稳定,故Z的氢化物比Y的氢化物稳定,故A错误;
B、同周期元素从左到右原子半径逐渐减小,同主族元素原子半径从上到下逐渐增大,则原子半径X>Y>R,故B正确;
C、三氧化硫不具有还原性,不可以被酸性高锰酸钾氧化,所以酸性高锰酸钾溶液不褪色,故C错误;
D、氯元素的高价氧化物的水化物HClO4的酸性最强,所以是Z元素最高价氧化物的水化物的酸性最强,故D错误;
故选B.
点评 本题考查位置结构性质的相互关系应用,难度中等,整体把握元素周期表的结构进行元素推断是解题关键.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
14.现有常温下的四种溶液(如表),下列有关叙述中正确的是( )
| ① | ② | ③ | ④ | |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
| A. | V1L④与V2L②溶液混合后,若混合后溶液pH=4,则V1:V2=9:11 | |
| B. | 由水电离出的c(H+):①=②=③=④ | |
| C. | 分别加水稀释10倍、四种溶液的pH:①>②>③>④ | |
| D. | 在①、②中分别加入适量的氯化铵晶体后,①的pH减小,②的pH不变 |
15.原子序数依次增大的X,Y,Z,W四种短周期元素,X,W原子的最外层电子数与其电子层数相等,X,Z的最外层电子数之和与Y,W的最外层电子数之和相等.甲的化学式为YX3,是一种具有刺激性气味的气体,乙是由X,Y,Z组成的盐.下列说法正确的是( )
| A. | 由X,Y,Z组成的盐的水溶液中阳离子总浓度大于阴离子总浓度 | |
| B. | YX3的水溶液呈弱碱性,能使湿润的蓝色石蕊试纸变红 | |
| C. | X与Z形成的化合物的水溶液可用于雕刻玻璃 | |
| D. | W的氯化物熔点低,易升华,但其水溶液能导电,由此推断它属于弱电解质 |
12. 有A、B、C、D、E五种元素.其相关信息如下:
有A、B、C、D、E五种元素.其相关信息如下:
请回答下列问题.
(1)写出E元素原子基态时的电子排布式1s22s22p63s23p63d104s1;
(2)C元素的第一电离能比氧元素的第一电离能大 (填“大”或“小”);
(3)CA3分子中C原子的杂化轨道类型是sp3;
(4)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有①③ (填序号)
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为a (填序号);
a.平面正方形 b.正四面体 c.三角锥型 d.V型
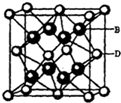
(5)B与D可形成离子化合物,其晶胞结构如图所示.其中D离子的配位数为8,若该晶体的密度为a g•cm-3,则该晶胞的体积是$\frac{\frac{78}{{N}_{A}}×4}{a}$cm3 (写出表达式即可).
 有A、B、C、D、E五种元素.其相关信息如下:
有A、B、C、D、E五种元素.其相关信息如下:| 元素 | 相关信息 |
| A | A原子的1s轨道上只有一个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道有三个未成对电子 |
| D | D为主族元素,且与E同周期,其最外层上有两个运动状态不同的电子 |
| E | E能形成红色(或砖红色)的E2O和EO两种氧化物 |
(1)写出E元素原子基态时的电子排布式1s22s22p63s23p63d104s1;
(2)C元素的第一电离能比氧元素的第一电离能大 (填“大”或“小”);
(3)CA3分子中C原子的杂化轨道类型是sp3;
(4)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有①③ (填序号)
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为a (填序号);
a.平面正方形 b.正四面体 c.三角锥型 d.V型
(5)B与D可形成离子化合物,其晶胞结构如图所示.其中D离子的配位数为8,若该晶体的密度为a g•cm-3,则该晶胞的体积是$\frac{\frac{78}{{N}_{A}}×4}{a}$cm3 (写出表达式即可).
19.下面关于化学反应的限度的叙述中,正确的是( )
| A. | 化学反应的限度都相同 | |
| B. | 化学反应的限度可以改变 | |
| C. | 可以通过延长化学反应的时间改变化学反应的限度 | |
| D. | 当一个化学反应在一定条件下达到限度时,反应即停止 |
9.下列化合物不能通过化合反应获得的是( )
| A. | Fe(OH)3 | B. | Al(OH)3 | C. | HCl | D. | NaHCO3 |
14.阿斯匹林的结构简式为: 则1mol阿斯匹林跟足量氢氧化钠溶液充分反应,消耗氢氧化钠的物质的量为( )
则1mol阿斯匹林跟足量氢氧化钠溶液充分反应,消耗氢氧化钠的物质的量为( )
 则1mol阿斯匹林跟足量氢氧化钠溶液充分反应,消耗氢氧化钠的物质的量为( )
则1mol阿斯匹林跟足量氢氧化钠溶液充分反应,消耗氢氧化钠的物质的量为( )| A. | 1mol | B. | 2mol | C. | 3mol | D. | 4mol |
 的名称为3,3,6-三甲基辛烷;
的名称为3,3,6-三甲基辛烷;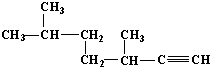 的名称为3,6-二甲基-1-庚炔;
的名称为3,6-二甲基-1-庚炔;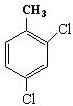 ;
; ,分子式为C15H22O2;
,分子式为C15H22O2;  中含有的官能团的名称为羟基,酯基.
中含有的官能团的名称为羟基,酯基.
 ;
;