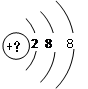题目内容
有关短周期元素A、B、C、D、E、F的信息如下:
| 元素 | 有关信息 |
| A | 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
| B | 最外层电子数是次外层电子数的2倍 |
| C | M层上有3个电子 |
| D | 短周期原子半径最大的主族元素 |
| E | 其单质是淡黄色固体 |
| F | 最高正价与最低负价代数和为6 |
请回答下列问题:
(1)写出实验室制取乙的化学方程式 。
(2)下列说法正确的是 (填序号)。
①实验室可用如图所示装置制取B的最高价氧化物
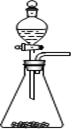
②用C单质做成的槽车,都可用来运输甲的浓溶液
③ C和铜与稀硫酸组成的原电池,C电极被还原
④ D单质在氧气中燃烧后的产物可用在防毒面具中作供氧剂
⑤鼓励乘坐公交车出行,倡导低碳生活,是控制和治理BO2解决“温室效应”的有效途径之一
 ⑥ DF的电子式为H∶Cl∶
⑥ DF的电子式为H∶Cl∶(3)将E的常见氧化物(该氧化物能使品红溶液褪色)通入由CuSO4和NaCl混合的浓溶液中,溶液颜色变浅,析出白色沉淀,取该沉淀进行元素质量分数分析,可知其中含Cl:35.7%,Cu:64.3%,则该氧化物在上述反应中的作用是 。
A.漂白剂 B.氧化剂 C.还原剂
(4)请用化学方法加以验证(3)中的氧化物,简要写出实验方法、试剂及预期可观察到的现象 。
(1)Ca(OH)2+2NH4Cl CaCl 2+2NH3↑+ 2H2O
CaCl 2+2NH3↑+ 2H2O
(2)①②④⑤ (少选1个得1分,少选2个或多选不得分)(3)C
(4)将适量气体样品通入品红溶液,溶液红色褪去,加热溶液,又恢复红色,说明气体为SO2(其他合理答案也可)
解析试题分析:A最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐,则A是氮元素,甲是硝酸,乙是氨气,生成的盐是硝酸铵。B最外层电子数是次外层电子数的2倍,则B一定是第二周期元素,是碳元素。C M层上有3个电子,所以C是Al元素。D短周期原子半径最大的主族元素,则D是Na元素。E其单质是淡黄色固体,所以E是S元素。F最高正价与最低负价代数和为6,这说明F是第ⅦA族元素,则F是氯元素。
(1)实验室制取氨气的化学方程式为Ca(OH)2+2NH4Cl CaCl 2+2NH3↑+ 2H2O。
CaCl 2+2NH3↑+ 2H2O。
(2)实验室用碳酸钙与盐酸反应制取CO2,属于固体与液体反应不需要加热的,因此装置图正确,①正确;常温下铝在浓硝酸中发生钝化,所以可以用铝单质做成的槽车,都可用来运输甲的浓溶液,②正确;铝的金属性强于铜,所以铝和铜与稀硫酸组成的原电池,铝电极是负极被氧化,③不正确;过氧化钠能和水以及CO2反应生成氧气,所以钠单质在氧气中燃烧后的产物可用在防毒面具中作供氧剂,④正确;鼓励乘坐公交车出行,倡导低碳生活,是控制和治理CO2解决“温室效应”的有效途径之一,⑤正确;钠和氯是活泼的金属与非金属,二者形成的化合物氯化钠是离子化合物,电子式为 ,⑥不正确,答案选①②④⑤。
,⑥不正确,答案选①②④⑤。
(3)将E的常见氧化物(该氧化物能使品红溶液褪色),这说明该氧化物是SO2。SO2通入由CuSO4和NaCl混合的浓溶液中,溶液颜色变浅,析出白色沉淀,取该沉淀进行元素质量分数分析,可知其中含Cl:35.7%,Cu:64.3%,则该沉淀中Cl与Cu的原子个数之比= :
: =1:1,所以其化学式为CuCl,即铜元素的化合价从+2价降低到+1价,这说明反应中硫酸铜起到氧化剂的作用,则SO2起到还原剂的作用,答案选C。
=1:1,所以其化学式为CuCl,即铜元素的化合价从+2价降低到+1价,这说明反应中硫酸铜起到氧化剂的作用,则SO2起到还原剂的作用,答案选C。
(4)SO2具有漂白性,能使品红溶液褪色,所以检验SO2的实验操作是将适量气体样品通入品红溶液,溶液红色褪去,加热溶液,又恢复红色,说明气体为SO2。
考点:考查元素周期表的结构以及核外电子排布;氨气、CO2制备;过氧化钠用途;原电池判断以及SO2的性质与检验等

(1)某短周期主族元素的原子M层上有一个半充满的亚层,这种原子的质子数是 ___________,写出它的外围电子排布图___________。
(2)VIA族的.硒(Se).在化合物中常表现出多种氧化态, H2SeO4比H2SeO3酸性_-___( 填强或弱),H2Se的酸性比H2S__________(填“强”或“弱”)。
(3)固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构,则下列有关说法中正确的是 ( )
| A.NH5中既有离子键又有共价键 |
| B.NH5的熔、沸点高于NH3 |
| C.NH5固体投入少量水中,可产生两种气体 |
| D.0.1 mol NH5中含有5 mol N—H键 |
现有部分短周期主族元素的有关信息,如下表:
| 元素编号 | T | X | Y | Z | W |
| 元素的性质或原子结构情况 | 短周期主族元素中原子半径最大 | 最外层上的电子数比次外层少1个且单质是气体 | 核外共有13种运动状态不同的电子 | 若低温蒸发液态空气,因其沸点较低可先获得它的单质 | 核外有5种不同能量的电子且其中有两个未成对的电子 |
(1)Y的最外层电子排布式是__ __,它的单质与碳生成的化合物与水反应生成甲烷和白色沉淀。写出该反应的化学方程式__ 。
(2)元素T的单质与水反应的离子方程式是 ,
在短周期主族元素中,X元素与其相邻元素的原子半径从小到大的顺序是_
(写元素符号)。
(3)W形成的一种单质,其式量为256,易溶于CS2,该单质的化学式为___ __,它属于_ ___晶体(写晶体类型)。
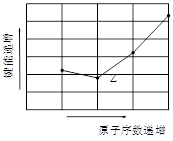
(4)如图为Z元素所在周期气态氢化物R-H键的键能大小,则该周期元素气态氢化物键能大小与键长的关系为_____ (用文字简述)。
A、B、C、D、E、F周表前四周期中的常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| A | A是周期表中原子半径最小的元素 |
| B | B元素的原子价电子排布为ns11np14 |
| C | M的基态原子L层电子数是K层电子数的3倍 |
| D | D是第三周期中第一电离能最小的元素 |
| E | E是地壳中含量最多的金属元素 |
| F | 有多种化合价,其某种高价阳离子的价电子具有较稳定的半充满结构 |
(1)F位于元素周期表中位置 ,其基态原子核外价电子排布式为 ;
(2)B的电负性比M的 (填“大”或“小”);B2A3分子中
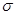 键与
键与 键与个数之比为 ;
键与个数之比为 ;(3)写出E的单质与D的最高价氧化物的水化物溶液反应的化学方程式: ;
(4)已知每5.4gE可与最低价F的氧化物反应,放出346.2kJ的热量。则请写出该反应的热化学方程式: 。
短周期元素A、B、C、D在元素周期表中的相对位置如图所示,其中B所处的周期序数与族序数相等。填写下列空白。
| | | A | |
| B | C | | D |
(1)写出C的氧化物的一种用途:
(2)B单质与Fe2O3反应时,每消耗13.5g B时放热213kJ,该反应的热化学方程式是
(3)为防止A元素的氧化物AO2污染空气,科学家寻求合适的化合物G和催化剂,以实现反应:
AO2+X催化剂A2 +H2O+n Z(未配平,n可以为0)。上述反应式中的X不可能是 (填标号)。
a.NH3 b.CO c.CH3CH2OH d.H2O2
(4)A元素的最简单氢化物甲、D元素的最高价氧化物对应的水化物乙都是很重要的基础化工原料。
①一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是 (选填序号)。
| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入H2的物质的量 | 加入甲的物质的量 |
| y | 甲的物质的量 | 平衡常数K | 甲的转化率 | 生成物物质的量总和 |
②25℃时,往a mol·L-1的甲的水溶液中滴加0.01 mol·L-1乙溶液,当两种溶液等体积混合时,溶液呈中性(设温度不变)。滴加过程中溶液的导电能力 (填“增强”、“减弱”或“不变”);
所得混合溶液中A、D两种元素的物质的量的关系为:A 2D(填“大于”、“等于”或“小于”);甲中溶质的电离平衡常数Kb= (用含a的代数式表示)。