题目内容
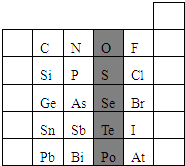
12.短周期元素W、X、Y和Z的原子序数依次增大.W是原子半径最小的元素,X原子的最外层电子数是内层电子数的2倍,Y元素原子的M层电子数比K层多1个,Z原子的最外层电子数是其电子层数的2倍.下列说法不正确的是( )| A. | 元素Z可与元素X形成共价化合物XZ2 | |
| B. | 元素X与W形成的原子个数比为1:1的化合物有很多种 | |
| C. | 元素W、X的氯化物中,各原子均满足8电子的稳定结构 | |
| D. | 元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 |
分析 短周期元素W、X、Y和Z的原子序数依次增大,W是原子半径最小的元素,则W为H元素;X原子的最外层电子数是其最内层电子数的2倍,则X原子有2个电子层,最外层电子数为4,则X为碳元素;Y元素原子的M层电子数比K层多1个,则Y为Na;Z原子的最外层电子数是其电子层数的2倍,原子有3个电子层,最外层电子数为6,故Z为S元素,据此解答.
解答 解:短周期元素W、X、Y和Z的原子序数依次增大,W是原子半径最小的元素,则W为H元素;X原子的最外层电子数是其最内层电子数的2倍,则X原子有2个电子层,最外层电子数为4,则X为碳元素;Y元素原子的M层电子数比K层多1个,则Y为Na;Z原子的最外层电子数是其电子层数的2倍,原子有3个电子层,最外层电子数为6,故Z为S元素.
A.元素Z可与元素X形化合物CS2,属于共价化合物,故A正确;
B.元素X与W形成的原子个数比为1:1的化合物有乙炔、苯、苯乙烯等,故B正确;
C.元素W、X的氯化物分别为HCl、CCl4,HCl中H原子不满足满足8电子的稳定结构,故C错误;
D.Na与氢氧化钠溶液或盐酸反应均有氢气生成,故D正确,
故选C.
点评 本题考查结构性质位置关系,难度不大,注意对基础知识的理解掌握.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
2.与Na+具有相同质子数和电子数的粒子是( )
| A. | F- | B. | NH4+ | C. | H2O | D. | CH4 |
3.咖啡鞣酸具有较广泛的抗菌作用,结构简式如图所示.下列关于咖啡鞣酸的说法中不正确的是( )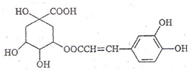

| A. | 分子式为C16H18O9 | |
| B. | 在一定条件下能发生消去反应 | |
| C. | 1mol咖啡鞣酸水解时可消耗8molNaOH | |
| D. | 与浓溴水既能发生取代反应又能发生加成反应 |
7.铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,下列说法正确的是( )
| A. | 铅蓄电池是新型的绿色环保电池 | |
| B. | 当电路中转移0.2mol电子时,消耗的H2SO4为0.2 mol | |
| C. | 铅蓄电池放电时负极质量减小,正极质量增加 | |
| D. | 铅蓄电池放电时电子由负极经过溶液定向移动到正极 |
17.如图是某品牌饮用矿泉水的标签的部分内容.下列说法正确的是( )


| A. | 标签上给出的离子的物理量是物质的量浓度 | |
| B. | 任何饮用水中氯离子(Cl-)的浓度均在10~27.3 mg/L之内 | |
| C. | 该品牌饮用矿泉水中c(Mg2+)最大值为2×10-4mol/L | |
| D. | 一瓶该品牌饮用矿泉水中SO42-的物质的量不超过1×10-5mol |
4.已知维生素A1的结构简式为: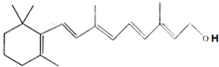 ,关于它的叙述正确的是( )
,关于它的叙述正确的是( )
 ,关于它的叙述正确的是( )
,关于它的叙述正确的是( )| A. | 维生素A1是一种易溶于水的醇 | |
| B. | 维生素A1分子中含有苯环结构 | |
| C. | 维生素A1能使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色,且原理相同 | |
| D. | 1mol维生素A1在催化剂作用下,最多与5molH2发生加成反应 |
1.哈伯因发明用氨气和氢气合成氨气的方法而获得1918年诺贝尔化学奖,现向一密闭容器中充入1molN2和3molH2,在一定条件下使该反应发生N2+3H2═2NH3.下列说法正确的是( )
| A. | 一定条件下达到化学平衡时,N2、H2和NH3的物质的量浓度之比为1:3:2 | |
| B. | 达到化学平衡时,N2完全转化为NH3 | |
| C. | 达到化学平衡时,正反应和逆反应速率相等,且都为零 | |
| D. | 单位时间内消耗amolN2同时消耗2amolNH3,说明该反应已达到平衡状态 |
2.25℃、101kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是
( )
( )
| A. | 2H2(g)+O2(g)═2H2O (l)△H=-285.8 kJ•mol-1 | |
| B. | 2H2(g)+O2(g)═2H2O (l)△H=+571.6 kJ•mol-1 | |
| C. | 2H2(g)+O2(g)═2H2O (g)△H=-571.6 kJ•mol-1 | |
| D. | H2(g)+1/2O2(g)═H2O (l)△H=-285.8 kJ•mol-1 |