题目内容
18.某学习小组通过查阅资料发现用KClO3和浓盐酸反应也可以制备氯气.为此该小组利用如图所示装置在实验室中制取Cl2并探究其相关性质: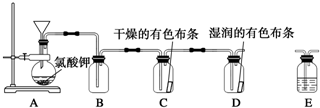
(1)装置A中存在一处错误,请改正这处错误:改长颈漏斗为分液漏斗.
(2)下列还可收集Cl2的正确装置是C.
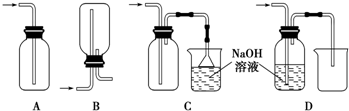
(3)为了除去氯气中的氯化氢,需要在装置A、B之间添加装置E,装置E中所盛装的试剂为饱和食盐水.为了探究使有色布条褪色的是氯气还是氯气与水反应的生成物,需要在整套装置中添加装置E,其中加入浓硫酸,装置E在整套装置中的添加位置为b(填序号).
a.A、B之间 b.B、C之间
c.C、D之间 d.D之后
(4)取下集气瓶B,将铁丝加热至红热状态,伸入到集气瓶B中,可以观察到的现象是集气瓶内和瓶口出现棕黄色烟,能检验该反应产物中铁元素价态的试剂是bcd(填序号).
a.氯水 b.蒸馏水和铁粉 c.氢氧化钠溶液 d.KSCN溶液
(5)另外一个化学学习小组就环境保护方面指出了上述装置的缺陷,并给出了改进措施,该改进措施是在装置D后增加一个盛装浓碱液的装置,使碱液吸收逸出的氯气尾气.
分析 (1)装置中反应试剂是浓盐酸易挥发,需要用分液漏斗加入;
(2)氯气密度大于空气密度,能够溶于水,易于氢氧化钠溶液反应;
(3)制备出的氯气含有挥发出的氯化氢,通过饱和食盐水可以除去,减小氯气的溶解性;探究使有色布条褪色的是氯气还是氯气与水反应的生成物,需要在整套装置中添加装置E,其中加入浓硫酸,应在C装置前干燥氯气;
(4)铁在氯气中燃烧发出棕黄色烟氯化铁;依据氯化铁性质分析三价铁离子结合氢氧根离子会生成红褐色沉淀,和铁反应生成氯化亚铁,溶液颜色发生改变,溶解后加入硫氰酸钾溶液呈血红色检验;
(5)氯气有毒,直接排放能够引起空气污染,氯气与氢氧化钠溶液反应,可以用氢氧化钠溶液吸收.
解答 解:(1)装置中反应试剂是浓盐酸易挥发,需要用分液漏斗加入,改长颈漏斗为分液漏斗,故答案:改长颈漏斗为分液漏斗;
(2)氯气密度大于空气密度,能够溶于水,易于氢氧化钠溶液反应;
A.没有出去空气,集气瓶容易发生爆炸,故A错误;
B.氯气密度大于空气密度,应选择向上排空气法收集,故B错误;
C.氯气密度大于空气密度,选择向上排空气法收集,氯气有毒用氢氧化钠吸收,应用防止倒吸装置,故C正确;
D.氯气与氢氧化钠溶液反应,收集不到氯气,故D错误;
故选:C;
(3)制备出的氯气含有挥发出的氯化氢,通过饱和食盐水可以除去,减小氯气的溶解性;探究使有色布条褪色的是氯气还是氯气与水反应的生成物,需要在整套装置中添加装置E,其中加入浓硫酸,应在C装置前干燥氯气,选择装置B、C之间;
故答案为:饱和食盐水;b;
(4)铁在氯气中燃烧,集气瓶内和瓶口出现棕黄色烟氯化铁;依据氯化铁性质分析三价铁离子结合氢氧根离子会生成红褐色沉淀,和铁反应生成氯化亚铁,溶液颜色发生改变,溶解后加入硫氰酸钾溶液呈血红色检验;
a.氯水,加入不出现明显现象,不能检验铁离子存在,故a不选;
b.蒸馏水和铁粉,用蒸馏水溶解氯化铁的溶液中加入铁反应溶液颜色变化为浅绿色,证明铁离子存在,故b正确;
c.蒸馏水和氢氧化钠溶液,用蒸馏水溶解氯化铁后加入氢氧化钠溶液会生成氢氧化铁红褐色沉淀,可以鉴别铁离子的存在,故c正确;
d.蒸馏水和KSCN溶液,用蒸馏水溶解氯化铁,加入KSCN溶液出现血红色溶液证明铁离子存在,故d正确;
故答案为:集气瓶内和瓶口出现棕黄色烟;bcd;
(5)氯气有毒,直接排放能够引起空气污染,应该在装置D后增加一个盛装浓碱液的装置,使碱液吸收逸出的氯气尾气;
故答案为:在装置D后增加一个盛装浓碱液的装置,使碱液吸收逸出的氯气尾气.
点评 本题考查了氯气的制备及性质检验,熟悉氯气制备原理及收集、净化、尾气处理装置的选择是解题关键,题目难度中等.

 阅读快车系列答案
阅读快车系列答案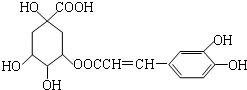
| A. | 分子式为C16H18O9 | |
| B. | 1mol咖啡鞣酸水解时可消耗8molNaOH | |
| C. | 咖啡鞣酸分子中所有原子都在同一平面上 | |
| D. | 与浓溴水既能发生取代反应又能发生加成反应 |
| A. | 次氯酸的电子式 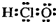 | |
| B. | S2-的结构示意图: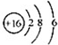 | |
| C. | 质子数为53,中子数为78的碘原子:13153I | |
| D. | NH4I的电子式: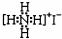 |
| A. | NH4+、Fe2+、NO3-、H+ | B. | K+、Mg2+、I-、ClO- | ||
| C. | K+、Ba2+、Cl-、Br- | D. | K+、HCO3-、Cl-、H+ |
| A. | 78% | B. | 22% | C. | 14% | D. | 13% |
| A. | Li | B. | S | C. | Si | D. | P |
①
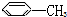 ②
②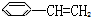 ③
③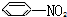 ④
④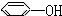 ⑤
⑤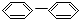 ⑥
⑥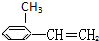
| A. | ③④ | B. | ②⑤⑥ | C. | ①②⑤⑥ | D. | ②③④⑤⑥ |
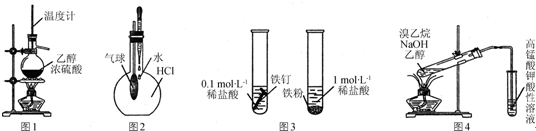
| A. | 用图1所示装置制取乙烯 | |
| B. | 用图2所示方法验证HCl气体易溶于水 | |
| C. | 用图3所示方法探究固体表面积对反应速率的影响 | |
| D. | 用图4所示方法检验溴乙烷与NaOH醇溶液共热产生乙烯 |