��Ŀ����
16����ȸʯ��Ҫ��Cu2��OH��2CO3�������������Ļ������Ļ�����Կ�ȸʯΪԭ�Ͽ��Ʊ�CuCl2•3H2O�����������ͼ��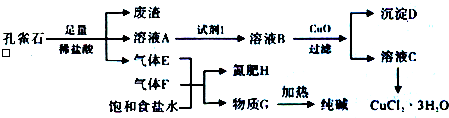
��֪����ҺAֻ��Cu2+��Fe2+��Fe3+���ֽ������ӣ����������ӳ�����pH���±���ʾ���ش��������⣺
| �������� | Fe3+ | Fe2+ | Cu2+ | |
| PH | �������↑ʼ���� | 1.9 | 7.0 | 4.7 |
| ����������ȫ���� | 3.2 | 9.0 | 6.7 | |
��2����ȸʯ����Ҫ�ɷ�������ϡ���ᷴӦ�Ļ�ѧ����ʽΪCu2��OH��2CO3+4HCl=2CuCl2+3H2O+CO2����
��3��ʹ����ͼ�С��Լ�1����Ŀ���ǽ���Һ�е�Fe2+ת��ΪFe3+���Լ�B��ѡ��BD����ѡ����ţ���
A������KMnO4��Һ B��˫��ˮ C��Ũ���� D����ˮ
��4������CuO�����ǵ�����ҺpH��ʹFe3+ת��Ϊ�������Է��룮��pH�ķ�ΧΪ3.2��pH��4.7��
��5������E��F�뱥��ʳ��ˮ��������H��Gʱ��E��FӦ��һ���Ⱥ�˳��ͨ�뱥��ʳ��ˮ�У����У�Ӧ��ͨ��������F��NH3������ż���Ӧ���ʵĻ�ѧʽ����
��6������ҺC���CuCl2•3H2O����Ҫ��������Ũ������ȴ�ᾧ�����˵Ȳ�����
��7����֪��������Cu��OH��2��Ksp=2��10-20������Cu2++2H2O?Cu��OH��2+2H+��Ӧƽ�ⳣ��5��10-9��
���� ���ȸʯ�м�������ϡ���ᣬ�����ķ�Ӧ��Cu2��OH��2CO3+4HCl=2CuCl2+3H2O+CO2������ҺAֻ��Cu2+��Fe2+��Fe3+���ֽ������ӣ���������������ϡ�����������Ρ������κ�ˮ��Ȼ����˵õ��������к���Si���������ҺA�к��к������κ������μ�CuCl2������EΪCO2��������CO2������F�ͱ���ʳ��ˮ��ϵõ�����H������G������Ԫ���غ�֪FΪNH3������HΪNH4Cl������G�õ������GΪNaHCO3��
����ҺA�м����Լ�1�õ���ҺB������ҺB�м���CuO�����˵õ���ҺC�ͳ���D������ҺC���ܵõ�CuCl2.3H2O�������DӦ�ú�����Ԫ�أ�CuO��Ŀ���ǵ�����Һ��pH��ʹFe 3+ת��ΪFe��OH��3����������Ԫ���غ�֪��B�к���Fe3+��Cu2+�����Լ�1��Ŀ���ǽ�Fe2+ת��ΪFe3+�Ҳ����������ʣ�Ӧ��ѡȡ˫��ˮ����ˮ���ݴ˷������
��� �⣺���ȸʯ�м�������ϡ���ᣬ�����ķ�Ӧ��Cu2��OH��2CO3+4HCl=2CuCl2+3H2O+CO2������ҺAֻ��Cu2+��Fe2+��Fe3+���ֽ������ӣ���������������ϡ�����������Ρ������κ�ˮ��Ȼ����˵õ��������к���Si���������ҺA�к��к������κ������μ�CuCl2������EΪCO2��������CO2������F�ͱ���ʳ��ˮ��ϵõ�����H������G������Ԫ���غ�֪FΪNH3������HΪNH4Cl������G�õ������GΪNaHCO3��
����ҺA�м����Լ�1�õ���ҺB������ҺB�м���CuO�����˵õ���ҺC�ͳ���D������ҺC���ܵõ�CuCl2.3H2O�������DӦ�ú�����Ԫ�أ�CuO��Ŀ���ǵ�����Һ��pH��ʹFe 3+ת��ΪFe��OH��3����������Ԫ���غ�֪��B�к���Fe3+��Cu2+�����Լ�1��Ŀ���ǽ�Fe2+ת��ΪFe3+�Ҳ����������ʣ�Ӧ��ѡȡ˫��ˮ����ˮ��
��1����Ӧ��ĽӴ����Խ��Ӧ����Խ�����Կ�ȸʯ��ĥ��Ŀ������������������Ӷ�����Ӧ���ʣ�
�ʴ�Ϊ����������������Ӷ�����Ӧ���ʣ�
��2����ȸʯ��ϡ���ᷴӦ�����Ȼ�ͭ��������̼��ˮ����Ӧ����ʽΪCu2��OH��2CO3+4HCl=2CuCl2+3H2O+CO2����
�ʴ�Ϊ��Cu2��OH��2CO3+4HCl=2CuCl2+3H2O+CO2����
��3�����Լ�1����Ŀ���ǽ���Һ�е�Fe2+ת��ΪFe3+���Ҳ����������ʣ���ѡBD��
��4������CuO�����ǵ�����ҺpH��ʹFe3+ת��Ϊ�������Է��룬�Ҳ��ܳ���������ͭ����������pHȡֵ��ΧΪ3.2��pH��4.7���ʴ�Ϊ��3.2��pH��4.7��
��5������E�Ƕ�����̼��F�ǰ�����̼������С�����ᣬ���Զ�����̼�����ڱ����Ȼ�����Һ��������������ˮ������Ӧ����ͨ��F��ΪNH3�����������̼���ܽ⣬�Ӷ�����̼�����ƺ��Ȼ�泥��ʴ�Ϊ��F��NH3��
��6������Һ�л�ȡ���壬Ӧ�ò�������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����ķ����õ��ϴ����ľ��壬�ʴ�Ϊ������Ũ������ȴ�ᾧ��
��7��������Cu��OH��2��Ksp=2��10-20����c��Cu 2+����c��OH-��2=Ksp=2��10-20��Cu2++2H2O?Cu��OH��2+2H+��Ӧƽ�ⳣ��K=$\frac{c��{H}^{+}��^{2}}{c��C{u}^{2+}��}$=$\frac{��\frac{{K}_{w}}{c��O{H}^{-}��}��^{2}}{c��C{u}^{2+}��}$=$\frac{{{K}_{w}}^{2}}{c��C{u}^{2+}����c��O{H}^{-}��^{2}}$=$\frac{{{K}_{w}}^{2}}{{K}_{sp}}$=$\frac{��1{0}^{-14}��^{2}}{2��1{0}^{-20}}$=5��10-9��
�ʴ�Ϊ��5��10-9��
���� ���⿼�������Ʊ������ʷ�����ᴿ��Ϊ�߿���Ƶ�㣬���ؿ���ѧ�����������㼰ʵ������������ؼ�����ȷʵ��ԭ������������������֪������ͼ�з����ķ�Ӧ�������������ѵ��ǣ�7���ļ��㣬Ҫ������֮���ת������Ŀ�Ѷ��еȣ�

| ���� | CH3COOH | HCN | H2CO3 |
| Ka | 1.8��10-8 | 4.9��10-10 | K1��4.3��10-7 K2��5.6��10-11 |
| A�� | �����ʵ���Ũ�ȵĸ���Һ��pH��ϵΪ��pH��NaCN����pH��Na2CO3����pH��CH3COONa�� | |
| B�� | a mol/L HCN��b mol/L NaOH��Һ�������Ϻ�������Һ��c��Na+����c��CN-������aһ��С��b | |
| C�� | ������������μ�ˮ����Һ���������������С | |
| D�� | NaHCO3��Na2CO3�Ļ��Һ�У�c��Na+��+c��H+��=c��OH-��+c��HCO3-��+c��CO32-�� |
| A�� | H2+2OH-=2H2O+2e- | B�� | O2+4H++4e-=2H2O | ||
| C�� | H2-2e-=2H+ | D�� | O2+2H2O+4e-=4OH- |
| A�� | MgSO4 | B�� | FeCl2 | C�� | AlCl3 | D�� | NaAlO2 |
| A�� | C5H12��2��ͬ���칹�� | |
| B�� | �ױ������ϵ�һ����ԭ�ӱ���3��̼ԭ�ӵ����ȡ�����������ʹ���6�� | |
| C�� | C8H10��ֻ���������ڷ�������ͬ���칹�� | |
| D�� | CH3CH2CH2CH3��������������Ӧ��ֻ����һ��һ�ȴ��� |
| A�� | 20g��ˮ��D2O�����еĵ�����Ϊ10 NA | |
| B�� | 46g NO2��N2O4�Ļ������������ԭ�Ӹ���Ϊ6.02��1023 | |
| C�� | 0.1mol����������������ˮ��Ӧ��ת�Ƶĵ�����Ϊ 0.2NA | |
| D�� | 1L 0.3 mol/LNa2SO4��Һ�У�����Na+��SO42-����Ϊ0.6 NA |



