题目内容
19.25℃时,弱酸的电离平衡常数如表:下列有关说法正确的是( )| 弱酸 | CH3COOH | HCN | H2CO3 |
| Ka | 1.8×10-8 | 4.9×10-10 | K1;4.3×10-7 K2:5.6×10-11 |
| A. | 等物质的量浓度的各溶液的pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) | |
| B. | a mol/L HCN与b mol/L NaOH溶液等体积混合后所得溶液中c(Na+)>c(CN-),则a一定小于b | |
| C. | 往冰醋酸中逐滴加水,溶液导电能力先增大,后减小 | |
| D. | NaHCO3和Na2CO3的混合液中:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
分析 A.酸的电离平衡常数越大,其酸根离子水解程度越小,则相同浓度的钠盐溶液pH越小;
B.等浓度、等体积的HCN和NaOH溶液混合,二者恰好反应生成NaCN,NaCN为强碱弱酸盐,其溶液呈碱性,再结合电荷守恒判断;
C.冰醋酸中逐渐加入水,促进醋酸电离,溶液的导电能力与离子浓度成正比;
D.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断.
解答 解:A.酸的电离平衡常数越大,其酸根离子水解程度越小,则相同浓度的钠盐溶液pH越小,电离平衡常数HCN<H2CO3<CH3COOH,所以水解程度CN->CO32->CH3COO-,则相同浓度的钠盐溶液pH大小顺序是:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa),故A错误;
B.等浓度、等体积的HCN和NaOH溶液混合,二者恰好反应生成NaCN,NaCN为强碱弱酸盐,其溶液呈碱性,则c (OH-)>c(H+),根据电荷守恒得c(Na+)>c(CN-),所以c(Na+)>c(CN-)时,则a不一定小于b,故B错误;
C.冰醋酸中逐渐加入水,促进醋酸电离,所以醋酸的电离程度逐渐增大,溶液的导电能力与离子浓度成正比,随着水的加入,氢离子浓度先增大后减小,溶液的导电能力先增大后减小,故C正确;
D.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),故D错误;
故选C.
点评 本题考查了离子浓度大小比较,涉及弱电解质的电离、盐类水解等知识点,根据溶质的性质结合电荷守恒来分析解答,易错选项是C,会分析加水稀释冰醋酸过程中各种粒子浓度变化、溶液导电能力变化等知识点,题目难度中等.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
9.某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子.在agHmX中所含质子的物质的量是( )
| A. | $\frac{a}{A(A-N+m)mol}$ | B. | $\frac{a}{A}$(A-N) mol | C. | $\frac{a}{A+m}$(A-N) mol | D. | $\frac{a}{A+m}$(A-N+m) mol |
14.R、M、T、G、J为原子序数依次递增的同一短周期主族元素,下列说法一定正确的是(m、n均为正整数)( )
| A. | 若M的最高正化合价为+4,则五种元素都是非金属元素 | |
| B. | HnJOm为强酸,则G是位于ⅤA族以后的活泼非金属元素 | |
| C. | 若T的最低化合价为-3,则J的最高正化合价为+7 | |
| D. | 若R、M的最高价氧化物的水化物均为碱,则R(OH)n的碱性一定比M(OH)n+1的碱性强 |
4.下列递变规律不正确的是( )
| A. | Na、Mg、Al还原性依次减弱 | B. | I2、Br2、Cl2氧化性依次增强 | ||
| C. | F、Cl、Br、I原子半径依次增大 | D. | N、O、F最高正价依次升高 |
11.下列关于铷的叙述中不正确的是( )
| A. | 它位于周期表的第四周期、第IA族 | |
| B. | 碳酸铷易加热分解为氧化铷和二氧化碳 | |
| C. | 铷的盐类大多易溶于水 | |
| D. | 氯化铷是离子化合物 |
8.下列物质反应后经过过滤,反应液质量增大的是( )
| A. | 少量铁粉加入AgNO3溶液中 | |
| B. | 少量Na2O2粉末加入CuSO4溶液中 | |
| C. | 少量BaSO4粉末加入饱和Na2CO3溶液中 | |
| D. | 少量Al2(SO4)3粉末加入Ba(OH)2溶液中 |
16.孔雀石主要含Cu2(OH)2CO3,还含少量铁的化合物和硅的化合物.以孔雀石为原料可制备CuCl2•3H2O及纯碱,流程如图.
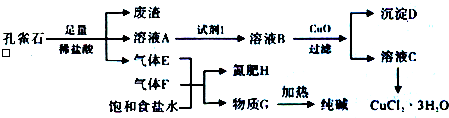
且知:溶液A只含Cu2+、Fe2+、Fe3+三种金属离子,且三种离子沉淀的pH如下表所示.回答下列问题:
(1)孔雀石研磨的目的是增大固体表面积,从而增大反应速率.
(2)孔雀石的主要成分与足量稀盐酸反应的化学方程式为Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑.
(3)使用上图中“试剂1”的目的是将溶液中的Fe2+转化为Fe3+,试剂B宜选用BD(填选项序号).
A.酸性KMnO4溶液 B.双氧水 C.浓硝酸 D.氯水
(4)加入CuO作用是调节溶液pH,使Fe3+转化为沉淀予以分离.则pH的范围为3.2≤pH<4.7.
(5)气体E、F与饱和食盐水作用生成H和G时,E和F应按一定先后顺序通入饱和食盐水中,其中,应先通入气体是F、NH3(填代号及对应物质的化学式).
(6)由溶液C获得CuCl2•3H2O,需要经过蒸发浓缩、冷却结晶、过滤等操作.
(7)已知:常温下Cu(OH)2的Ksp=2×10-20.计算Cu2++2H2O?Cu(OH)2+2H+反应平衡常数5×10-9.

且知:溶液A只含Cu2+、Fe2+、Fe3+三种金属离子,且三种离子沉淀的pH如下表所示.回答下列问题:
| 金属离子 | Fe3+ | Fe2+ | Cu2+ | |
| PH | 氢氧化物开始沉淀 | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀 | 3.2 | 9.0 | 6.7 | |
(2)孔雀石的主要成分与足量稀盐酸反应的化学方程式为Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑.
(3)使用上图中“试剂1”的目的是将溶液中的Fe2+转化为Fe3+,试剂B宜选用BD(填选项序号).
A.酸性KMnO4溶液 B.双氧水 C.浓硝酸 D.氯水
(4)加入CuO作用是调节溶液pH,使Fe3+转化为沉淀予以分离.则pH的范围为3.2≤pH<4.7.
(5)气体E、F与饱和食盐水作用生成H和G时,E和F应按一定先后顺序通入饱和食盐水中,其中,应先通入气体是F、NH3(填代号及对应物质的化学式).
(6)由溶液C获得CuCl2•3H2O,需要经过蒸发浓缩、冷却结晶、过滤等操作.
(7)已知:常温下Cu(OH)2的Ksp=2×10-20.计算Cu2++2H2O?Cu(OH)2+2H+反应平衡常数5×10-9.