��Ŀ����
7����Ч̼��������ҹ�����������һ�����ͻ��ʣ���ҵ����̼����淋Ĺ�������������ʾ��
��������ش��������⣺
��1���������жಽ��ɣ�������ȴ�����ˡ�ϴ�ӡ����ʵ���ҽ��й��˲����õ��IJ����������ձ���©������������
��2�����빤���ǽ����ӷ�Ӧ������з�������������ԭ�������˰�����Һ�����ʣ����ѭ�����Ŀ�������ԭ�����������ʣ�
��3�������������������̣�Ŀ���dz�ȥ�����е�SO2�����壬ʵ���ҽ��д˲�����ѡ�õ��Լ���ad����д��ţ���
a��NaHCO3��Һ b��NaOH��Һc��Ca��OH��2��Һd��KMnO4������Һ
��4��ʵ����ʵ���������̿���������װ���е�cd����д��ţ���

��5������ά����������ú��1898�꣬ʩ���ţ�Schlosing���������̼����粒������Ȼ��Ʊ�����Һ��������̼�������ټ����ƴ���ķ�����
��д������̼�����ƵĻ�ѧ����ʽ��NH4HCO3+NaCl=NaHCO3��+NH4Cl��
�ڲⶨʩ���ŷ����ɵ�̼��������Ʒ��̼�����Ƶ������������ֱ��ȡmg��Ʒ�������飬���з��������������b ����д��ţ���
a���������������ͨ����ˮ����װ�á��ռ�������n L������ɱ����
b�����ȡ���ȴ���ܽ������BaCl2�����ˡ�ϴ�ӡ��������������Ϊn g
c���ܽ�������̪��ָʾ������w mol/LNaOH��Һ�ζ�������NaOH n mL
d���������������ͨ����ʯ�ҡ�������ʯ������n g
��Ʒ��̼�����Ƶ���������Ϊ$\frac{16800n}{197m}%$���ú�m��n��w��n��m�Ĵ���ʽ��ʾ����
���� ��1��ʵ���ҽ��й��˲����õ��IJ����������ձ���©������������
��2��������Һ�������淴Ӧ�У�ԭ����ѭ��ʹ�ÿ������ԭ�������ʣ�
��3��������������Ҫ����ͨ�������̼�������壬���Գ�ȥ����������ѡ��ǿ�Ӧѡ�ò��������̼��Ӧ��̼�����ƺ�KMnO4������Һ���գ�
��4��������������ˮ������ʱ��Ҫ��ֹ������
��5����̼����粒���ͱ����Ȼ�����Һ�������ܽ�Ȳ�ͬ��Ӧ����̼�����Ƴ������Ȼ�泥�
��a����Ʒ�п��ܺ���NH4HCO3���Ҷ�����̼��������ˮ�����ʣ�ͨ����ˮ���ռ��õ��Ķ�����̼�������ʵ�����ɵĶ�����̼��������ȣ�
b����������Ϊn g���˹���������������ɵ�̼�ᱵ������������̼�ᱵ��������̼���Ƶ�����������̼���ƿ�������̼�����Ƶ���������������̼�����Ƶ�����������
c��̼��������Һ�Լ��ԣ����������Ƶζ�����̪��ɫ���ᷢ���仯��
d����Ʒ�п��ܺ���NH4HCO3���Ҽ�ʯ�ҿ�������ˮ�������ʼ�ʯ�����ӵ��������ڶ�����̼��������
���ù�ϵʽ�����м��㣬2NaHCO3��Na2CO3��CaCO3��BaCO3��
��� �⣺��1��ʵ���ҽ��й��˲����õ��IJ����������ձ���©������������
�ʴ�Ϊ���ձ���©������������
��2����������ǽ����ӷ�Ӧ������з�������������ԭ�������˰���ѹ��Һ����ΪҺ�壬��Ӧ�ǿ��淴Ӧ����ԭ��������������ѭ��ʹ�����ԭ�������ʣ�
�ʴ�Ϊ����Һ�������ԭ�����������ʣ�
��3��������������Ҫ����ͨ�������̼�������壬���Գ�ȥ����������ѡ��ǿ���bc��ѡ��
̼�����ơ�KMnO4������Һ�������ն����������������̼����Ӧ����ad��ѡ��
�ʴ�Ϊ��ad��
��4��������������ˮ������ʱ��Ҫ��ֹ������
abװ��ˮֱ�����հ���������������ab��ѡ��
cװ�ò��ö����������ȫ��������������c��ѡ��
dװ�ð������������Ȼ�̼���������б�ˮ��ȫ���շ�ֹ�˵�������d��ѡ��
�ʴ�Ϊ��cd��
��5������̼����粒������Ȼ��Ʊ�����Һ��������̼�����ƣ���Ӧ�Ļ�ѧ����ʽΪ��NH4HCO3+NaCl=NaHCO3��+NH4Cl��
�ʴ�Ϊ��NH4HCO3+NaCl=NaHCO3��+NH4Cl��
��a���������������ͨ����ˮ����װ�á��ռ�������n L������ɱ��������Ʒ�п��ܺ���NH4HCO3���Ҷ�����̼��������ˮ�����ʣ�ͨ����ˮ���ռ��õ��Ķ�����̼�������ʵ�����ɵĶ�����̼��������ȣ���a��������
b�����ȡ���ȴ���ܽ������BaCl2�����ˡ�ϴ�ӡ��������������Ϊn g���˹���������������ɵ�̼�ᱵ������������̼�ᱵ��������̼���Ƶ�����������̼���ƿ�������̼�����Ƶ���������������̼�����Ƶ�������������b������
c���ܽ�������̪��ָʾ������w mol/LNaOH��Һ�ζ�������NaOH n mL��̼��������Һ�Լ��ԣ����������Ƶζ�����̪��ɫ���ᷢ���仯����c��������
d���������������ͨ����ʯ�ҡ�������ʯ������n g����Ʒ�п��ܺ���NH4HCO3���Ҽ�ʯ�ҿ�������ˮ�������ʼ�ʯ�����ӵ��������ڶ�����̼����������d��������
2NaHCO3��Na2CO3��CaCO3��BaCO3
168 197
xg ng
$\frac{168}{197}=\frac{xg}{ng}$��
��ã�x=$\frac{168n}{197}$��
����Ʒ��̼�����Ƶ���������Ϊ$\frac{\frac{168n}{197}}{m}��100%$=$\frac{16800n}{197m}%$��
�ʴ�Ϊ��b��$\frac{16800n}{197m}%$��
���� �����Գ�Ч̼����淋�����Ϊ���忼��ʵ�鷽������Ƽ����ۣ���Ŀ�Ѷ��еȣ��˽ⳣ�õ����ʷ��뷽����ʵ����������ǽ���Ĺؼ���

 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д�| A�� | ��λ�����ڱ��ĵ������ڡ���IA�� | |
| B�� | ̼������ȷֽ�Ϊ����墨Ͷ�����̼ | |
| C�� | 卑�������������ˮ | |
| D�� | �Ȼ�������ӻ����� |
| A�� | �������ۼ���AgNO3��Һ�� | |
| B�� | ����Na2O2��ĩ����CuSO4��Һ�� | |
| C�� | ����BaSO4��ĩ���뱥��Na2CO3��Һ�� | |
| D�� | ����Al2��SO4��3��ĩ����Ba��OH��2��Һ�� |
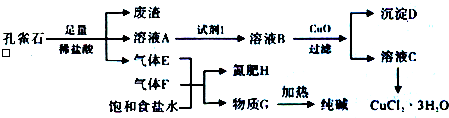
��֪����ҺAֻ��Cu2+��Fe2+��Fe3+���ֽ������ӣ����������ӳ�����pH���±���ʾ���ش��������⣺
| �������� | Fe3+ | Fe2+ | Cu2+ | |
| PH | �������↑ʼ���� | 1.9 | 7.0 | 4.7 |
| ����������ȫ���� | 3.2 | 9.0 | 6.7 | |
��2����ȸʯ����Ҫ�ɷ�������ϡ���ᷴӦ�Ļ�ѧ����ʽΪCu2��OH��2CO3+4HCl=2CuCl2+3H2O+CO2����
��3��ʹ����ͼ�С��Լ�1����Ŀ���ǽ���Һ�е�Fe2+ת��ΪFe3+���Լ�B��ѡ��BD����ѡ����ţ���
A������KMnO4��Һ B��˫��ˮ C��Ũ���� D����ˮ
��4������CuO�����ǵ�����ҺpH��ʹFe3+ת��Ϊ�������Է��룮��pH�ķ�ΧΪ3.2��pH��4.7��
��5������E��F�뱥��ʳ��ˮ��������H��Gʱ��E��FӦ��һ���Ⱥ�˳��ͨ�뱥��ʳ��ˮ�У����У�Ӧ��ͨ��������F��NH3������ż���Ӧ���ʵĻ�ѧʽ����
��6������ҺC���CuCl2•3H2O����Ҫ��������Ũ������ȴ�ᾧ�����˵Ȳ�����
��7����֪��������Cu��OH��2��Ksp=2��10-20������Cu2++2H2O?Cu��OH��2+2H+��Ӧƽ�ⳣ��5��10-9��
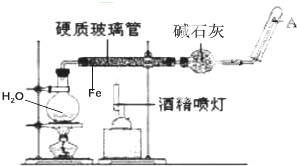 ��ͼ���ڸ����£�Fe��ˮ�����ķ�Ӧʵ�飮
��ͼ���ڸ����£�Fe��ˮ�����ķ�Ӧʵ�飮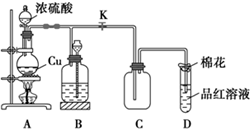 ��1��װ��A�з�����Ӧ�Ļ�ѧ����ʽΪCu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
��1��װ��A�з�����Ӧ�Ļ�ѧ����ʽΪCu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��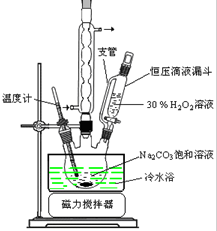 2Na2CO3•3H2O2��һ�����͵���ϵƯ����ijʵ����ȤС�����������ʵ�飮
2Na2CO3•3H2O2��һ�����͵���ϵƯ����ijʵ����ȤС�����������ʵ�飮 ��
��