题目内容
【题目】下表列出了①~⑩十种元素在周期表中的位置:
ⅠA | ||||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
请按要求回答下列问题。
(1)元素⑧对应的简单离子的结构示意图是____________。
(2)以上元素中,化学性质最不活泼的是 ____________(填元素符号)。
(3)写出元素⑤形成的单质在空气中燃烧的化学方程式______________________,这一反应是____________(填“吸热”或“放热”)反应。
(4)用电子式表示④与⑤形成的A2B型化合物的形成过程___________________________。
(5)在这些元素的最高价氧化物对应水化物中,酸性最强的化合物的分子式是:__________,与元素⑥的最高价氧化物对应水化物发生反应时的离子方程式为________________
(6)③的简单氢化物与③的最高价氧化物对应的水化物反应的生成物中含有的的化学键有____________________________。
【答案】 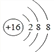 Ar 2Na +O2
Ar 2Na +O2 ![]() Na2O2 放热
Na2O2 放热 ![]() HClO4 Al(OH)3 +3H+= Al 3++ 3H2O 离子键、共价键
HClO4 Al(OH)3 +3H+= Al 3++ 3H2O 离子键、共价键
【解析】根据元素在周期表中的位置可知,①为H;②为C;③为N;④为O;⑤为Na;⑥为Al;⑦为P;⑧为S;⑨为Cl;⑩为Ar。
(1)元素⑧为S,是16号元素,简单阴离子的结构示意图为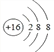 ,故答案为:
,故答案为: ;
;
(2)以上元素中,化学性质最不活泼的是Ar,故答案为:Ar;
(3)钠在空气中燃烧生成过氧化钠,反应的化学方程式为2Na +O2 ![]() Na2O2,物质的燃烧反应属于放热反应,故答案为:2Na +O2
Na2O2,物质的燃烧反应属于放热反应,故答案为:2Na +O2 ![]() Na2O2;放热;
Na2O2;放热;
(4)氧化钠的形成过程用电子式表示为![]() ,故答案为:
,故答案为:![]() ;
;
(5)元素的非金属性越强,最高价氧化物对应水化物的酸性越强,酸性最强的化合物的分子式是HClO4,与氢氧化铝反应的离子方程式为Al(OH)3 +3H+= Al 3++ 3H2O,故答案为:HClO4;Al(OH)3 +3H+= Al 3++ 3H2O;
(6)N的简单氢化物与N的最高价氧化物对应的水化物反应的生成物为硝酸铵,其中含有的的化学键有离子键、共价键,故答案为:离子键、共价键。

 阅读快车系列答案
阅读快车系列答案