题目内容
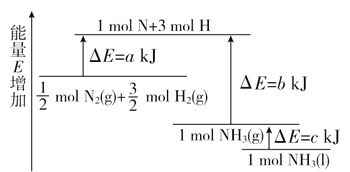
【题目】化学反应N2+3H2===2NH3的能量变化如图所示,该反应的热化学方程式是( )
A. ![]() N2(g)+
N2(g)+![]() H2(g)=NH3(l) ΔH=(a-b-c) kJ/mol
H2(g)=NH3(l) ΔH=(a-b-c) kJ/mol
B. N2(g)+3H2(g)=2NH3(g) ΔH=2(b-a) kJ/mol
C. ![]() N2(g)+
N2(g)+![]() H2(g)=NH3(l) ΔH=(b+c-a) kJ/mol
H2(g)=NH3(l) ΔH=(b+c-a) kJ/mol
D. ![]() N2(g)+
N2(g)+![]() H2(g)=NH3(g) ΔH=(a+b) kJ/mol
H2(g)=NH3(g) ΔH=(a+b) kJ/mol
【答案】A
【解析】由图示可知断裂0.5 mol N2(g)和1.5 mol H2(g)中的化学键共吸收a kJ的能量,由1 mol N和3 mol H生成1 mol NH3(g)放出b kJ的能量,由1 mol NH3(g)变为1 mol NH3(l)放出c kJ能量;由0.5 mol N2(g)和1.5 mol H2(g)生成1 mol NH3(g)或1 mol NH3(l)均放出能量。故有①N2(g)+H2(g)![]() NH3(g)ΔH=-(b-a)kJ·mol-1=(a-b)kJ·mol-1或②N2(g)+H2(g)
NH3(g)ΔH=-(b-a)kJ·mol-1=(a-b)kJ·mol-1或②N2(g)+H2(g)![]() NH3(l)ΔH=-(b+c-a)kJ·mol-1=(a-b-c)kJ·mol-1,因此C、D项均错误,A选项正确;将①式乘以2得:N2(g)+3H2(g)
NH3(l)ΔH=-(b+c-a)kJ·mol-1=(a-b-c)kJ·mol-1,因此C、D项均错误,A选项正确;将①式乘以2得:N2(g)+3H2(g)![]() 2NH3(g)ΔH=2(a-b)kJ·mol-1,B错误;答案选A。
2NH3(g)ΔH=2(a-b)kJ·mol-1,B错误;答案选A。

【题目】下表列出了①~⑩十种元素在周期表中的位置:
ⅠA | ||||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
请按要求回答下列问题。
(1)元素⑧对应的简单离子的结构示意图是____________。
(2)以上元素中,化学性质最不活泼的是 ____________(填元素符号)。
(3)写出元素⑤形成的单质在空气中燃烧的化学方程式______________________,这一反应是____________(填“吸热”或“放热”)反应。
(4)用电子式表示④与⑤形成的A2B型化合物的形成过程___________________________。
(5)在这些元素的最高价氧化物对应水化物中,酸性最强的化合物的分子式是:__________,与元素⑥的最高价氧化物对应水化物发生反应时的离子方程式为________________
(6)③的简单氢化物与③的最高价氧化物对应的水化物反应的生成物中含有的的化学键有____________________________。