��Ŀ����
����Ŀ��A��B��C��D��E�����ֶ���������Ԫ�أ�����A��Ԫ�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�B���γɻ�������������Ԫ�أ�C�ǵؿ��к�������Ԫ�أ�D����̬�⻯���ˮ��Һ�Լ��ԣ�E�����Ƴɽ�������ӹ����Ƴ�һ�ָ������ķ��⾵���ý�����ĩ����������ϳ����ں��Ӹֹ죮
(1)д��C��E��Ԫ�ط���______��______��
(2)BԪ��λ�����ڱ��е�λ��Ϊ______��BC2�ĵ���ʽΪ______(��Ԫ�ط��ű�ʾ)��
(3)A��B��C��D��ԭ�Ӱ뾶�ɴ�С��˳��Ϊ______(��Ԫ�ط��ű�ʾ)��
(4)E������������Ӧ��ˮ�����������Ԫ��������������Ӧˮ���������ǿ����������Һ�з�Ӧ�����ӷ���ʽ______��
���𰸡�O Al �ڶ�����IVA�� ![]() C��N��O��H Al��OH��3+OH��=AlO2��+2H2O
C��N��O��H Al��OH��3+OH��=AlO2��+2H2O
��������
A��B��C��D��E�����ֶ���������Ԫ�أ�����A��Ԫ�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ���AΪHԪ�أ�B���γɻ�������������Ԫ�أ���BΪCԪ�أ�C�ǵؿ��к�������Ԫ�أ���CΪOԪ�أ�D����̬�⻯���ˮ��Һ�Լ��ԣ���DΪNԪ�أ�E�����Ƴɽ�������ӹ����Ƴ�һ�ָ������ķ��⾵���ý�����ĩ����������ϳ����ں��Ӹֹ죬��EΪAl��
��1��CΪOԪ�ء�EΪAlԪ�أ��ʴ�Ϊ��O��Al��
��2��BΪ̼Ԫ�أ�λ�����ڱ��е�λ��Ϊ���ڶ�����IVA�壬CO2�ĵ���ʽΪ![]() ���ʴ�Ϊ���ڶ�����IVA�壻
���ʴ�Ϊ���ڶ�����IVA�壻![]() ��
��
��3������Ԫ����Hԭ�Ӱ뾶��С��ͬ�����������ԭ�Ӱ뾶��С����ԭ�Ӱ뾶��C��N��O��H���ʴ�Ϊ��C��N��O��H��
��4��E������������Ӧ��ˮ����ΪAl��OH��3��������Ԫ��������������Ӧˮ���������ǿ������ΪNaOH����������Һ�з�Ӧ�����ӷ���ʽ��Al��OH��3+OH��=AlO2��+2H2O��
�ʴ�Ϊ��Al��OH��3+OH��=AlO2��+2H2O��

����Ŀ��PCl3��Ҫ��������аٳ���л���ũҩ�ͻǰ����(S.D)��ҽҩ��ԭ�ϡ���ͼΪʵ��������ȡ��PCl3��Ʒ��װ�ã��г�װ����ȥ��
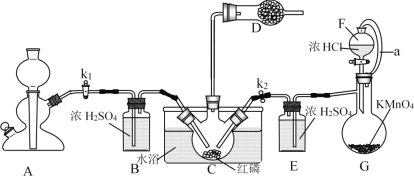
����������֪������������Cl2��Ӧ����PCl3�������Cl2��Ӧ����PCl5��PCl3��ˮ��ǿ��ˮ������H3PO3��PCl3��O2������POCl3(��������)��PCl3��POCl3���۷е���±���
���� | �۵�/�� | �е�/�� |
PCl3 | -112 | 75.5 |
POCl3 | 2 | 105.3 |
�ش��������⣺
(1)����G��������______��װ��F��G����a����ͨ��a��������_______��
(2)A����ȡCO2װ�ã�CO2��������_____��ѡ��A�е�ҩƷ��_____(����ĸ)��
a.ϡ���� b.ϡ���� c.NaHCO3��ĩ d.��״ʯ��ʯ
(3)װ��D��ʢ�м�ʯ�ң���������__________________��
(4)װ��G������Cl2����Ӧ�����ӷ���ʽΪ___________��
(5)װ��C����65-70��ˮԡ���ȣ��Ƶõ�PCl3�ֲ�Ʒ�г�����POCl3��PCl5�����ʣ����ӵķ����ǣ��ȼ�������ȣ���ȥPCl5��Ȼ��ͨ��___________(��ʵ���������)�����ɵõ��ϴ�����PCl3��
(6)ͨ��ʵ��ⶨ�ֲ�Ʒ��PCl3������������ʵ�鲽������(���������ʵķ�Ӧ)��
��һ����Ѹ����ȡ20.0 g PCl3�ֲ�Ʒ����ˮ��ȫˮ��������500mL��Һ��
�ڶ�������ȡ25.00mL��Һ������ƿ�У�
������������0. 5molL��1����Һ20mL���������H3PO3��ȫ��Ӧ����H3PO4��
���IJ������뼸�ε�����Һ����1.0 molL��1Na2S2O3����Һ�ζ������ĵ⣬��Ӧ����ʽΪI2+2Na2S2O3=Na2S4O6+2NaI�������յ�ʱ����Na2S2O3����Һ12mL��
�ٵ������з�Ӧ�Ļ�ѧ����ʽΪ_____________��
�ڸ����������ݣ�����ò�Ʒ��PCl3����������Ϊ______%��
����Ŀ��ij����С�������ͼ��ʾװ����ȡ�϶���������������֪������ˮ�Ȼ��ƿ����Ҵ��γ�������ˮ��CaCl2��6C2H5OH��
���й��л���ķе㣺
�Լ� | ���� | �Ҵ� | ���� | �������� |
�е㣨�棩 | 34.7 | 78.5 | 118 | 77.1 |
����˵����ȷ����
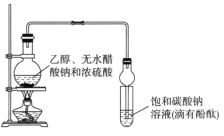
A.װ�������ιܼ��������������ܷ�ֹ����
B.��Ӧ��������Թ��е������ǣ���Һ�ֲ㣬�²���ɫ��״Һ�壻�ϲ���Һ��ɫ��dz
C.�Ӵ��Թ��з���������������л�����һ�������Ҵ������Ѻ�ˮ��Ӧ�ȼ�����ˮ�Ȼ��ƣ����˷�����Ҵ�
D.��������ˮ�����ƣ�Ȼ����������ռ�118�����ҵ���֣��Եõ��ϴ���������������