��Ŀ����
4��������Һ�п��ܺ���SO42-��SO32-��S2-��Cl-��Br-��I-��NO3-��Na+��Mg2+�����ӣ���1��������ˮ����Һ����ɫ��Ϊ�ػ�ɫ�������ֻ��ǣ�����Һ��һ������S2-��I-��
��2�������Ȼ�����Һ������Ļ����Һ�������ɣ����ȼ�����ˮ��Ȼ���ټ����Ȼ�����Һ�����ᣬ�а�ɫ�������ɣ���ԭ��Һ��һ������SO32-��
��3������������������Һ�������ɣ�������������ҺҲ�������ɣ���ԭ��Һ������������ֻ������NO3-��Na+��
���� ��1��������ˮ����Һ����ɫ��Ϊ�ػ�ɫ�������ֻ��ǣ����ɵij���ΪS���ʣ���ҺΪ�ػ�ɫ��˵�������˵ⵥ�ʣ�
��2�������Ȼ�����Һ������Ļ����Һ�������ɣ���һ����������������ӣ����ȼ�����ˮ��Ȼ���ټ����Ȼ�����Һ�����ᣬ�а�ɫ�������ɣ�˵����Һ��һ����������������ӣ�
��3������������������Һ�������ɣ�����Һ�в���������������ӡ���������ӣ�������������ҺҲ�������ɣ�����Һ�в����������ӡ������Ӻ͵����ӣ���ֻ�ܴ�����������Ӻ������ӣ�
��� �⣺��1��������ˮ����Һ����ɫ��Ϊ�ػ�ɫ��˵����Ӧ���ɵĵⵥ�ʣ���Һ��һ������I-�����ֻ��ǣ�˵�����ɵij�����ֻ��ΪS���ʣ�����Һ��һ������S2��
�ʴ�Ϊ��S2-��I-��
2�������Ȼ�����Һ������Ļ����Һ�������ɣ���һ��������SO42-�����ȼ�����ˮ��Ȼ���ټ����Ȼ�����Һ�����ᣬ�а�ɫ�������ɣ��ð�ɫ����Ϊ���ᱵ��˵����Һ��һ������SO32-��
�ʴ�Ϊ��SO32-��
��3������������������Һ�������ɣ�����Һ�в�����SO42-��SO32-��������������ҺҲ�������ɣ�����Һ�в�����Cl-��Br-��I-����ֻ�ܴ���NO3-��Na+��
�ʴ�Ϊ��NO3-��Na+��
���� ���⿼���˳������ӵļ��鷽������Ŀ�Ѷ��еȣ���ȷ�������ӵ����ʼ����鷽��Ϊ���ؼ���ע���������ӷ�Ӧ����������������ӹ����жϴ��ڵ����ӣ�������ؿ���ѧ���ķ���������������������

 �����Ƹ���ʦ����ϵ�д�
�����Ƹ���ʦ����ϵ�д� ��ͨ����ͬ����ϰ��ϵ�д�
��ͨ����ͬ����ϰ��ϵ�д�| A�� | ��ϩ��������7���Ҽ���2���м� | |
| B�� | ��60 g SiO2�����У�Si-O������ĿΪ2NA | |
| C�� | ���ۼ��з����ԣ����ޱ����� | |
| D�� | �ɢ�A��͢�A��Ԫ���γɵ�ԭ�Ӹ�����Ϊ1��1����������Ϊ38�Ļ�����Ǻ��й��ۼ������ӻ����� |
| A�� | 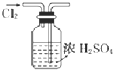 �������� | B�� |  ����K2CO3�е�K+ | ||
| C�� | 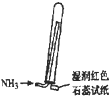 �ռ�������NH3������ | D�� |  �Ʊ�Fe��OH��2 |
| Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
| T | M������2�ԳɶԵ��� |
| X | �����������Ǵ�����������2�� |
| Y | �����µ���Ϊ˫ԭ�ӷ��ӣ����⻯��ˮ��Һ�ʼ��� |
| Z | Ԫ�����������+7�� |
��2��Ԫ��Y����Ԫ���γ�һ������YH${\;}_{4}^{+}$��д�������ĵ���ʽ
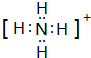 ����Ԫ�ط��ű�ʾ����
����Ԫ�ط��ű�ʾ������3��Ԫ��Z��Ԫ��T��ȣ��ǽ����Խ�ǿ����Cl����Ԫ�ط��ű�ʾ�������б�������֤����һ��ʵ����bef��
a��������Z�ĵ��ʺ�T�ĵ���״̬��ͬ
b��Z���⻯���T���⻯���ȶ�
c��һ��������Z��T�ĵ��ʶ���������������Һ��Ӧ
d��Zԭ�ӵļ۵�������Tԭ�Ӷ�
e��Z������������ˮ��������ǿ��T������������ˮ���
f��Z�ĵ�������T���⻯��ˮ��Һ�����û���Ӧ
��4��Z�ж��ֳ��������ᣬ������ǿ������˳����HClO4��HClO3��HClO��
| A�� | Һ̬�������д����������������ӱ��Ȼ�����ȶ� | |
| B�� | ��̼����ԭ���γɵĻ�����Ƚ��ʯӲ������Ҫԭ����̼������̼̼������ | |
| C�� | S8��NO2���ǹ��ۻ����NH4Cl��CaC2�������ӻ����� | |
| D�� | ����AijԪ�ص�ԭ������Ϊm����ͬ���ڢ�AԪ�ص�ԭ�������п���Ϊm+10 |
| A�� | ����ϡ����ķ�Ӧ | |
| B�� | ���ȵ�ľ̿��CO2��Ӧ | |
| C�� | �����������е�ȼ�շ�Ӧ | |
| D�� | Ba��OH��2•8H2O������NH4Cl����ķ�Ӧ |
| A�� | NH3 | B�� | ��ϩ | C�� | ���� | D�� | ��ϩ |
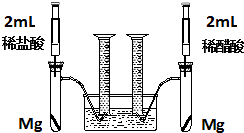 ʵ��һ��ij��ѧС��Ϊ�Ƚ�����ʹ�������ԣ����������ʵ�鷽����װ����ͼ��
ʵ��һ��ij��ѧС��Ϊ�Ƚ�����ʹ�������ԣ����������ʵ�鷽����װ����ͼ��