题目内容
14.下列说法正确的是( )| A. | 丙烯分子中有7个σ键,2个π键 | |
| B. | 在60 g SiO2晶体中,Si-O键的数目为2NA | |
| C. | 共价键有方向性,但无饱和性 | |
| D. | 由ⅠA族和ⅥA族元素形成的原子个数比为1:1、电子总数为38的化合物,是含有共价键的离子化合物 |
分析 A.根据丙烯的结构简式CH3-CH=CH2判断;
B.计算物质的量,结合二氧化硅含有四个Si-O键判断;
C.s-sσ键没有方向性;
D.由ⅠA族和ⅥA族元素形成的原子个数比为1:1、电子总数为38的化合物,该化合物为Na2O2.
解答 解:A.C-C、C-H键均为σ键,C=C中一个σ键,一个π键,则丙烯分子有8个σ键,1个π键,故A错误;
B.60 g SiO2物质的量=$\frac{60g}{60g/mol}$=1mol,硅形成四个Si-O键,60g水晶晶体中,含有“Si-O”键的数目为4NA,故B错误;
C.s-sσ键没有方向性,化学键都有饱和性,故C错误;
D.由ⅠA族和ⅥA族元素形成的原子个数比为1:1、电子总数为38的化合物,该化合物为Na2O2,为离子化合物,含有非极性共价键,故D正确.
故选D.
点评 本题考查化学键,为高频考点,把握化学键的形成、分类及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意结合实例分析,题目难度不大.

练习册系列答案
 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案 互动课堂系列答案
互动课堂系列答案
相关题目
4.以下物质间的每步转化通过一步反应能实现的是( )
| A. | Al→Al2O3→Al(OH)3→NaAlO2 | B. | Si→SiO2→H2SiO3→Na2SiO3 | ||
| C. | N2→NO→NO2→HNO3 | D. | S→SO3→H2SO4→MgSO4 |
2.下列分子的中心原子形成sp2杂化轨道的是( )
| A. | H2O | B. | NH3 | C. | C2H4 | D. | CH4 |
9.如图是生活中常用的锌锰干电池的示意图,下列有关说法中不正确的是( )


| A. | 电池负极反应为:Zn-2e-═Zn2+ | B. | 锌是负极,碳棒是正极 | ||
| C. | 电子由碳棒经外电路流向锌 | D. | 锌锰干电池属一次电池 |
19.在一定温度下,反应H2(g)+Br2(g)?2HBr(g),达到平衡的标志是( )
| A. | 容器里的压强不随时间的变化而改变 | |
| B. | 单位时间内生成2mol HBr的同时,消耗1 mol H2 | |
| C. | 单位时间内生成2mol HBr的同时,生成1 mol H2 | |
| D. | 正反应和逆反应速率都相等,都等于0 |
6.下列解释实验事实的方程式正确的是( )
| A. | 常温下反应4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)的△H>0,△S<0 | |
| B. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应,放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)$?_{500℃、30MPa}^{催化剂}$2NH3(g),△H=-38.6 kJ•mol-1 | |
| C. | FeCl3溶液中通入SO2,溶液黄色褪去:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | |
| D. | 向苯酚钠溶液中通入CO2,溶液变浑浊:2C6H5O-+CO2+H2O-→2C6H5OH↓+CO32- |
3.下表为元素周期表的一部分,请回答有关问题:
(1)⑥和⑧的元素符号分别是S、Ar;
(2)表中最活泼的金属是K,非金属最强的元素是F; (填写元素符号)
(3)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:在NaBr溶液中通入氯气(或加入氯水),溶液变红棕色(或橙色).
(4)比较③、④、⑨三种元素的金属性(或非金属性)强弱K>Mg>Al,判断的依据是(有反应方程式的请写涉及的化学方程式及必要的文字描述)2K+2H2O=2KOH+H2,剧烈反应,Mg+2H2O $\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2+H2,缓慢反应,而金属铝与水在加热条件下反应不明显,结论:金属性K>Mg>Al.
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 4 | ⑨ | ⑩ |
(2)表中最活泼的金属是K,非金属最强的元素是F; (填写元素符号)
(3)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:在NaBr溶液中通入氯气(或加入氯水),溶液变红棕色(或橙色).
(4)比较③、④、⑨三种元素的金属性(或非金属性)强弱K>Mg>Al,判断的依据是(有反应方程式的请写涉及的化学方程式及必要的文字描述)2K+2H2O=2KOH+H2,剧烈反应,Mg+2H2O $\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2+H2,缓慢反应,而金属铝与水在加热条件下反应不明显,结论:金属性K>Mg>Al.
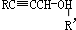
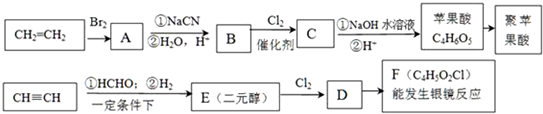
 .
.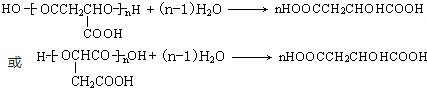 .
.