��Ŀ����
16����֪��ӡ������ʱ�ײ�������������Ũ�ȹ���ʱ�������к�����������ǿ�����ԣ�����ʹʪ��ĵ⻯�ص�����ֽ���������г�������ת��Ϊ��������1��д������ƽ������Ӧ�����ӷ���ʽO3+2I-+H2O=2OH-+I2+O2��
��2���÷�Ӧ����������O3����ԭ������OH-��
��3���÷�Ӧ�������ַ�Ӧ����������ӦΪI-ת��ΪI2���ڻ�ԭ��Ӧ���̵ķ�ӦʽΪO3+H2O+2e-�T2OH-+O2��
��4����Ӧ��1mol�����õ�����õ�����ʧȥ����2mol���ӣ�
���� ��1���������������������ɵⵥ�ʣ�ͬʱ���ֳ���ת��Ϊ�������÷�Ӧ��OԪ�ػ��ϼ���0�۱�Ϊ-2�ۡ�IԪ�ػ��ϼ���-1�۱�Ϊ0�ۣ�
��2���÷�Ӧ��OԪ�ػ��ϼ���0�۱�Ϊ-2�ۡ�IԪ�ػ��ϼ���-1�۱�Ϊ0�ۣ��õ��ӻ��ϼ۽��͵ķ�Ӧ��������������������Ӧ�IJ����ǻ�ԭ���
��3��������ԭ��Ӧ����������Ӧ��һ����������Ӧ��һ���ǻ�ԭ��Ӧ���õ��ӵ����ʷ�����ԭ��Ӧ��ʧ���ӵ����ʷ���������Ӧ��
��4����Ӧ�в��ֳ�����OԪ�ػ��ϼ��ڷ�Ӧ����0�۱�Ϊ-2�ۣ����ݷ���ʽ֪���μӷ�Ӧ��$\frac{1}{3}$�����ڷ�Ӧ�еõ��ӣ�
��� �⣺��1����������ǿ�����ԣ��ܺ͵����ӷ�Ӧ���ɵ�������������в���OԪ�ػ��ϼ���0�۱�Ϊ-2�ۡ���Ԫ�ػ��ϼ���-1�۱�Ϊ0�ۣ�ͬʱ��Һ�л��������������ӣ�����ת�Ƶ����غ���ԭ���غ���ƽ����ʽΪO3+2I-+H2O=2OH-+I2+O2���ʴ�Ϊ��O3+2I-+H2O=2OH-+I2+O2��
��2����������ԭ��Ӧ�еõ��ӻ��ϼ۽��͵ķ�Ӧ������������ʧ���ӻ��ϼ����ߵķ�Ӧ���ǻ�ԭ������������Ӧ�IJ����ǻ�ԭ�����ԭ����Ӧ�IJ�����������������в���OԪ�ػ��ϼ���0�۱�Ϊ-2�ۡ���Ԫ�ػ��ϼ���-1�۱�Ϊ0�ۣ�����O3������������ԭ������OH-��
�ʴ�Ϊ��O3�� OH-��
��3��������ԭ��Ӧ����������Ӧ��һ����������Ӧ��һ���ǻ�ԭ��Ӧ���õ��ӵ����ʷ�����ԭ��Ӧ��ʧ���ӵ����ʷ���������Ӧ������I-����������Ӧת��ΪI2�������õ��ӷ�����ԭ��Ӧ�������������ӣ���ӦʽΪO3+H2O+2e-�T2OH-+O2��
�ʴ�Ϊ��I-��I2��O3+H2O+2e-�T2OH-+O2��
��4����Ӧ�в��ֳ�����OԪ�ػ��ϼ��ڷ�Ӧ����0�۱�Ϊ-2�ۣ����ݷ���ʽ֪���μӷ�Ӧ��$\frac{1}{3}$�����ڷ�Ӧ�еõ��ӣ������1mol�����μӷ�Ӧ���õ����ӵ����ʵ���=1mol��$\frac{1}{3}$��3��[0-��-2��]=2mol��
�ʴ�Ϊ���õ���2��
���� �����Գ���Ϊ���忼��������ԭ��Ӧ�����ؿ����������������ۣ�ע��÷�Ӧ�����������ij���ռ�μӷ�Ӧ��$\frac{1}{3}$��Ϊ�״��㣮

| A�� | �����·�Ӧ4Fe��OH��2��s��+2H2O��l��+O2��g���T4Fe��OH��3��s���ġ�H��0����S��0 | |
| B�� | 500�桢30 MPa�£���0.5 mol N2��1.5 mol H2�����ܱ������г�ַ�Ӧ������19.3 kJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��$?_{500�桢30MPa}^{����}$2NH3��g������H=-38.6 kJ•mol-1 | |
| C�� | FeCl3��Һ��ͨ��SO2����Һ��ɫ��ȥ��2Fe3++SO2+2H2O�T2Fe2++SO42-+4H+ | |
| D�� | ������Һ��ͨ��CO2����Һ����ǣ�2C6H5O-+CO2+H2O-��2C6H5OH��+CO32- |
| A�� | ������Һ | B�� | ������ | ||
| C�� | FeCl3��Һ | D�� | ���Ƶ�Cu��OH��2��������Һ |
| A�� | NaHCO3��Һ | B�� | KSCN��Һ | C�� | NaOH��Һ | D�� | NH3•H2O��Һ |
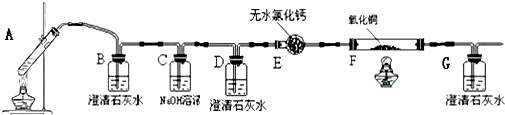
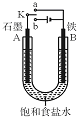 ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮
ij����С��ͬѧ����ͼװ�ý���ʵ�飬�Իش��������⣮ ������Ԫ��ԭ�Ӱ뾶�Ӵ�С��˳����Na��Si��O��F��H ����Ԫ�ط��ţ���
������Ԫ��ԭ�Ӱ뾶�Ӵ�С��˳����Na��Si��O��F��H ����Ԫ�ط��ţ���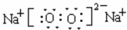 ��
�� ��
��