题目内容
【题目】化学反应的焓变通常用实验进行测定,也可理论推算,回答下列问题。
(1)实验测得,1 g CH3OH(l)在氧气中充分燃烧生成二氧化碳和液态水释放出22.7kJ的热量,试写出甲醇燃烧的热化学方程式_______________________________________。
(2)已知某工业生产中甲烷与水蒸汽存在如下反应:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) △H1
ii.CO(g)+H2O(g)=CO2(g)+H2(g) △H2
iii.CH4(g)=C(s)+2H2(g) △H3
……
Iii为积炭反应,利用△H1和△H2计算△H3时,还需要利用_____________反应的△H。(写化学方程式)
(3)氯化氢转化为氯气的催化过程如下:
CuCl2(s)=CuCl(s)+![]() Cl2(g) △H1=+83 kJ·mol-1
Cl2(g) △H1=+83 kJ·mol-1
CuCl(s)+![]() O2(g)=CuO(s)+
O2(g)=CuO(s)+![]() Cl2(g) △H2=-20 kJ·mol-1
Cl2(g) △H2=-20 kJ·mol-1
CuO(s)+2HCl(g)= CuCl2(s)+H2O(g) △H3=-121 kJ·mol-1
则4HCl(g)+ O2(g)= 2Cl2(g)+2H2O(g)的△H=___________kJ·mol-1
【答案】2CH3OH(l)+ 3O2(g)= 2CO2 (g)+4H2O(l) △H=-1452.8kJ/mol C(s)+2 H2O(g)=CO2(g)+2H2(g)或C(s)+CO2(g)=2 CO(g) -116
【解析】
(1) 1 g完全燃烧释放22.7kJ,2mol甲醇的质量为64g,释放的热量为1452.8kJ;
(2)根据盖斯定律计算;
(3)根据盖斯定律计算。
(1) CH3OH(l)在氧气中充分燃烧生成二氧化碳和液态水的方程式为2CH3OH(l)+ 3O2(g)= 2CO2 (g)+4H2O(l), 1 g完全燃烧释放22.7kJ,2mol甲醇的质量为64g,释放的热量为1452.8kJ,则热化学方程式为2CH3OH(l)+ 3O2(g)= 2CO2 (g)+4H2O(l) △H=-1452.8kJ/mol;
(2)根据盖斯定律,i+ ii- iii可得,C(s)+2 H2O(g)=CO2(g)+2H2(g),或i- ii- iii可得,C(s)+CO2(g)=2 CO(g),还缺少此反应的焓变。
(3)根据盖斯定律,①CuCl2(s)=CuCl(s)+![]() Cl2(g) △H1=+83 kJ·mol-1② CuCl(s)+
Cl2(g) △H1=+83 kJ·mol-1② CuCl(s)+![]() O2(g)=CuO(s)+
O2(g)=CuO(s)+![]() Cl2(g) △H2=-20 kJ·mol-1③CuO(s)+2HCl(g)= CuCl2(s)+H2O(g) △H3=-121 kJ·mol-1,(①+②+③)×2即可得到4HCl(g)+ O2(g)= 2Cl2(g)+2H2O(g),则△H=-116kJ/mol。
Cl2(g) △H2=-20 kJ·mol-1③CuO(s)+2HCl(g)= CuCl2(s)+H2O(g) △H3=-121 kJ·mol-1,(①+②+③)×2即可得到4HCl(g)+ O2(g)= 2Cl2(g)+2H2O(g),则△H=-116kJ/mol。

 教学练新同步练习系列答案
教学练新同步练习系列答案【题目】中科院一项最新成果实现了甲烷高效生产乙烯,甲烷在催化作用下脱氢,在气相中经自由基偶联反应生成乙烯,其反应如下: 2CH4(g) ![]() C2H4(g) +2H2(g) ΔH>0
C2H4(g) +2H2(g) ΔH>0
化学键 | H—H | C—H | C = C | C—C |
E(kJ / mol) | a | b | c | d |
(1)已知相关化学键的键能如上表,甲烷制备乙烯反应的ΔH=___________ (用含a.b.c.d的代数式表示)。
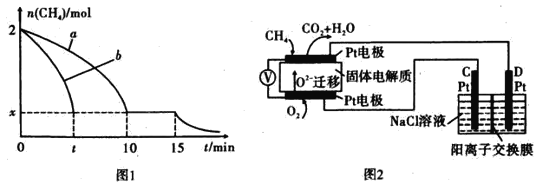
(2)T1温度时,向1 L的恒容反应器中充入2 molCH4 ,仅发生上述反应,反应过程中 0~15 min CH4的物质的量随时间变化如图1所示,测得10-15 min时H2的浓度为1.6 mol/L。
①0~ 10 min内CH4表示的反应速率为____mol/(Lmin) o
②若图中曲线a、曲线b分别表示在温度T1时,使用质量相同但表面积不同的催化剂时,达到平衡过程中n (CH4)变化曲线,其中表示催化剂表面积较大的曲线是 ________ (填"a"或 “b”)。
③15 min时,若改变外界反应条件,导致n( CH4)发生图中所示变化,则改变的条件可能是_____(任答一条即可)。
(3)实验测得v正=k正c2(CH4),v逆=k逆c(C2H4).c2(H2) 其中K正、K逆为速率常数仅与温度有关,T1温度时k正与K逆的比值为______ (填数值)。若将温度由T1升高到T2,则反应速率增大的倍数V正 ____V逆(填“>”“=”或“<”),判断的理由是__________
(4)科研人员设计了甲烷燃料电池并用于电解。如图2所示,电解质是掺杂了 Y2O3与 ZrO2的固体,可在高温下传导O2-
①C极的Pt为_______ 极(选填“阳”或“阴” )。
②该电池工作时负极反应方程式为_____________________ 。
③用该电池电解饱和食盐水,一段时间后收集到标况下气体总体积为112 mL,则阴极区所得溶液c(OH—)=_______ (假设电解前后溶液的体积均为500 mL)。