题目内容
(1)钠在高温条件下能与氢气化合成白色的NaH,反应的化学方程式为 ,
(2)NaH能与水剧烈反应:NaH+H2O═NaOH+H2↑,NaH与液氨(NH3)也有类似反应,写出该反应的化学方程式 .如果有12g NaH参加此反应,则转移电子的个数为 .
(2)NaH能与水剧烈反应:NaH+H2O═NaOH+H2↑,NaH与液氨(NH3)也有类似反应,写出该反应的化学方程式
考点:钠的化学性质,钠的重要化合物
专题:元素及其化合物
分析:(1)根据题干信息反应物为钠和氢气,生成物为氢化钠,依据质量守恒定律书写化学方程式;
(2)NaH中Na为+1价,则H为-1价,具有还原性,与水反应生成氢气和NaOH,为H元素之间发生氧化还原反应,水为氧化剂,与液氨(NH3)也有类似反应,所以NH3作氧化剂,根据化合价的变化计算电子的转移数目;
(2)NaH中Na为+1价,则H为-1价,具有还原性,与水反应生成氢气和NaOH,为H元素之间发生氧化还原反应,水为氧化剂,与液氨(NH3)也有类似反应,所以NH3作氧化剂,根据化合价的变化计算电子的转移数目;
解答:
解:(1)钠在高温条件下能与氢气化合成白色的NaH,所以反应物为钠和氢气,生成物为氢化钠,发生的反应为:2Na+H2
2NaH,
故答案为:2Na+H2
2NaH;
(2)NaH中Na为+1价,则H为-1价,为最低价态,可被氧化,具有还原性,NaH能与水剧烈反应:NaH+H2O═NaOH+H2↑,水为氧化剂,与液氨(NH3)也有类似反应,所以NH3作氧化剂,NaH中-1价H变为生成物中0价的氢,1个氢转移1个电子,氨气中需1个氢原子从+1价变为0价,根据得失电子守恒和质量守恒,反应方程式为:NaH+NH3═NaNH2+H2↑,12g NaH的物质的量为n=
=
=0.5mol,NaH中-1价H变为生成物中0价的氢,1个氢原子转移1个电子,则
0.5molNaH转移电子的个数为0.5NA,
故答案为:NaH+NH3═NaNH2+H2↑;0.5NA;
| ||
故答案为:2Na+H2
| ||
(2)NaH中Na为+1价,则H为-1价,为最低价态,可被氧化,具有还原性,NaH能与水剧烈反应:NaH+H2O═NaOH+H2↑,水为氧化剂,与液氨(NH3)也有类似反应,所以NH3作氧化剂,NaH中-1价H变为生成物中0价的氢,1个氢转移1个电子,氨气中需1个氢原子从+1价变为0价,根据得失电子守恒和质量守恒,反应方程式为:NaH+NH3═NaNH2+H2↑,12g NaH的物质的量为n=
| m |
| M |
| 12g |
| 24g/mol |
0.5molNaH转移电子的个数为0.5NA,
故答案为:NaH+NH3═NaNH2+H2↑;0.5NA;
点评:本题考查氧化还原反应,为高考高频考点,注意从元素化合价的角度认识氧化还原反应的相关概念和物质的性质,注意NaH中Na为+1价,则H为-1价,具有还原性,题目难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,22.4L氯气与足量的氢氧化钠溶液反应转移的电子数为NA |
| B、22.4L氨气中原子总数为4NA |
| C、标准状况下,22.4L SO3的分子数为NA |
| D、0.1mol/L CaCl2溶液中含有0.2NA个Cl- |
下列有关物质的性质和应用的说法中正确的是( )
| A、二氧化硫和氯水均具有漂白性,混合使用效果更好 |
| B、对滴有酚酞试液的CH3COONa溶液加热,溶液的颜色将变浅 |
| C、新能源汽车的推广与使用有助于减少光化学烟雾的产生 |
| D、用脱硫处理的煤代替原煤做燃料可以有效减少空气中CO2气体的含量 |
意大利科学家最近合成了一种新型的氧分子,其化学式为O4,对其说法正确的是( )
| A、O4是一种化合物 |
| B、O4是由O2组成的混合物 |
| C、O4是一种单质 |
| D、一个O4分子由2个O2分子构成 |
下列离子方程式正确的是( )
| A、小苏打溶液中加入醋酸:HCO3-+H+═CO2↑+H2O |
| B、碳酸氢铵溶液和足量氢氧化钠溶液混合:NH4++OH-═NH3?H2O |
| C、NaHS水解:HS-+H2O═S2-+H3O+ |
| D、硫酸亚铁溶液中滴加酸化的双氧水:2Fe2++2H++H2O2═2Fe3++2H2O |
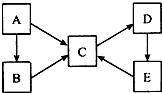 A、B、C、D、E五种物质均含有同一种元素,它们之间的转化关系如图所示:
A、B、C、D、E五种物质均含有同一种元素,它们之间的转化关系如图所示: