题目内容
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,22.4L氯气与足量的氢氧化钠溶液反应转移的电子数为NA |
| B、22.4L氨气中原子总数为4NA |
| C、标准状况下,22.4L SO3的分子数为NA |
| D、0.1mol/L CaCl2溶液中含有0.2NA个Cl- |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氯气与氢氧化钠溶液的反应中,氯气既是氧化剂也是还原剂,1mol氯气完全反应转移了1mol电子;
B.没有告诉在标准状况下,不能使用标况下的气体摩尔体积计算氨气的物质的量;
C.标准状况下,三氧化硫不是气体,不能使用标况下的气体摩尔体积计算三氧化硫的物质的量;
D.缺少氯化钙溶液的体积,无法计算溶液中氯离子的数目.
B.没有告诉在标准状况下,不能使用标况下的气体摩尔体积计算氨气的物质的量;
C.标准状况下,三氧化硫不是气体,不能使用标况下的气体摩尔体积计算三氧化硫的物质的量;
D.缺少氯化钙溶液的体积,无法计算溶液中氯离子的数目.
解答:
解:A.标况下22.4L氯气的物质的量为1mol,1mol氯气与氢氧化钠溶液反应转移了1mol电子,转移的电子数为NA,故A正确;
B.不是标准状况下,题中条件无法计算22.4L氨气的物质的量,故B错误;
C.标准状况下,三氧化硫不是气体,题中条件无法计算22.4L三氧化硫的物质的量,故C错误;
D.没有告诉氯化钙溶液的体积,无法计算溶液中氯离子的物质的量,故D错误;
故选A.
B.不是标准状况下,题中条件无法计算22.4L氨气的物质的量,故B错误;
C.标准状况下,三氧化硫不是气体,题中条件无法计算22.4L三氧化硫的物质的量,故C错误;
D.没有告诉氯化钙溶液的体积,无法计算溶液中氯离子的物质的量,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件,选项D为易错点,注意题中缺少溶液体积.

练习册系列答案
相关题目
电化学在日常生活中用途广泛,下图①是镁、次氯酸钠燃料电池的示意图,电池总反应式为:Mg+ClO-+H2O═Cl-+Mg(OH)2↓,图②是含Cr2O72-工业废水的电化学处理示意图.下列说法正确的是( )
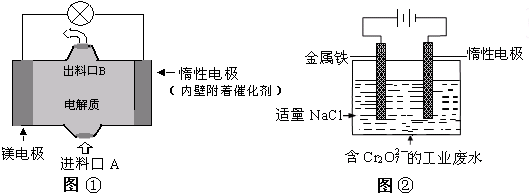

| A、图②中Cr2O72-离子向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去 |
| B、图②中阳极上的电极反应式为:Fe-3e-═Fe3+ |
| C、图①中发生的还原反应是:Mg2++ClO-+H2O+2e-═Cl-+Mg (OH)2↓ |
| D、若图①中3.6g镁溶解产生的电量用以图②废水处理,理论可产生10.7g氢氧化铁沉淀 |
在25℃时,用蒸馏水稀释1mol/L氨水至0.01mol/L,随溶液的稀释,下列各项中始终保持增大趋势的是( )
A、
| ||||
B、
| ||||
C、
| ||||
| D、OH-物质的量 |
下列溶液中的Cl-浓度与50mL 1mol/L MgCl2溶液中的Cl-浓度相等的是( )
| A、150mL 2mol/L KCl溶液 |
| B、75mL 1mol/L CaCl2溶液 |
| C、150mL 1mol/L NaCl溶液 |
| D、75mL 1mol/L AlCl3溶液 |
下列属于电解质的一组是( )
①CuSO4 ②氧化钠 ③水银 ④SO3 ⑤氯水 ⑥酒精 ⑦NaOH.
①CuSO4 ②氧化钠 ③水银 ④SO3 ⑤氯水 ⑥酒精 ⑦NaOH.
| A、①⑦ | B、①②⑦ |
| C、①④⑦ | D、①③⑤⑦ |
氢气是人类最理想的能源.已知在25℃、101kPa下,1g氢气完全燃烧生成液态水时放出热量142.9kJ,则下列热化学方程式书写正确的是( )
| A、2H2+O2═2H2O;△H=-142.9kJ/mol |
| B、2H2(g)+O2(g)═2H2O(l);△H=-142.9kJ/mol |
| C、2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ/mol |
| D、2H2(g)+O2(g)═2H2O(l);△H=+571.6kJ/mol |
下列说法正确的是( )
| A、氮原子的质量就是氮的相对原子质量 |
| B、氢氧化钠的摩尔质量是40g |
| C、氩气的摩尔质量在数值上等于它的相对原子质量 |
| D、1mol H2SO4中含有1mol H2 |