题目内容
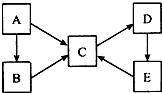 A、B、C、D、E五种物质均含有同一种元素,它们之间的转化关系如图所示:
A、B、C、D、E五种物质均含有同一种元素,它们之间的转化关系如图所示:(1)若A为单质,B、C均属于盐类,B的水溶液呈酸性,C的水溶液呈碱性,D是一种白色沉淀.写出下列过程的离子方程式:
①B的水溶液呈酸性
②C→D
③E→C
(2)若A~E均为化合物.A是淡黄色固体;B、C两溶液在等物质的量浓度时,C 溶液的pH较小,电解D的水溶液是最重要的工业生产之一,D→E→C也是工业制备C的普遍方法.
①A的电子式为
②电解D的水溶液时,反应的离子方程式为
③生铁浸入D溶液而发生锈蚀,正极的电极反应为
(3)若A为单质,C、D的相对分子质量相差16,0.1mol/L E溶液中只有3种离子,且常温下溶液中的
| c(H+) |
| c(OH-) |
①B→C的化学方程式为:
②A→C的反应中,每转移1mol e-就会吸热45kJ,写出该反应的热化学方程式:
考点:无机物的推断
专题:推断题
分析:A、B、C、D、E五种物质均含有同一种元素,
(1)若A为单质,B、C均属于盐类,B的水溶液呈酸性,C的水溶液呈碱性,D是一种白色沉淀,A为金属单质,A为Al、B为强酸弱碱盐、C为NaAlO2、D为Al(OH)3、E为Al2O3,再结合题目解答;
(2)若A~E均为化合物.A是淡黄色固体,能发生反应生成B、C,则A是Na2O2,过氧化钠能和水、二氧化碳分别反应生成NaOH、Na2CO3,B、C两溶液在等物质的量浓度时,C 溶液的pH较小,则B是NaOH、C是Na2CO3,电解D的水溶液是最重要的工业生产之一,则D为NaCl,D→E→C也是工业制备C的普遍方法,则E是NaHCO3;
(3)若A为单质,C、D的相对分子质量相差16,相差一个O原子,0.1mol/L E溶液中只有3种离子,且常温下溶液中的
=1012,溶液呈强酸性,E为酸,符合条件时,A为N2、B为NH3、C为NO、D为NO2、E为HNO3,再结合物质之间的反应分析解答.
(1)若A为单质,B、C均属于盐类,B的水溶液呈酸性,C的水溶液呈碱性,D是一种白色沉淀,A为金属单质,A为Al、B为强酸弱碱盐、C为NaAlO2、D为Al(OH)3、E为Al2O3,再结合题目解答;
(2)若A~E均为化合物.A是淡黄色固体,能发生反应生成B、C,则A是Na2O2,过氧化钠能和水、二氧化碳分别反应生成NaOH、Na2CO3,B、C两溶液在等物质的量浓度时,C 溶液的pH较小,则B是NaOH、C是Na2CO3,电解D的水溶液是最重要的工业生产之一,则D为NaCl,D→E→C也是工业制备C的普遍方法,则E是NaHCO3;
(3)若A为单质,C、D的相对分子质量相差16,相差一个O原子,0.1mol/L E溶液中只有3种离子,且常温下溶液中的
| c(H+) |
| c(OH-) |
解答:
解:A、B、C、D、E五种物质均含有同一种元素,
(1)若A为单质,B、C均属于盐类,B的水溶液呈酸性,C的水溶液呈碱性,D是一种白色沉淀,A为金属单质,A为Al、B为强酸弱碱盐、C为NaAlO2、D为Al(OH)3、E为Al2O3,
①B为强酸弱碱盐,铝离子水解生成氢氧化铝和氢离子,导致溶液呈酸性,水解方程式为Al3++3H2O?Al(OH)3+3H+,故答案为:Al3++3H2O?Al(OH)3+3H+;
②C是偏铝酸钠,D是氢氧化铝,偏铝酸钠和酸反应生成氢氧化铝沉淀,离子方程式为AlO2-+H++H2O=Al(OH)3↓,故答案为:AlO2-+H++H2O=Al(OH)3↓;
③E是氧化铝、C是偏铝酸钠,氧化铝和氢氧化钠溶液反应生成偏铝酸钠和水,离子方程式为Al2O3+2OH-=2AlO2-+H2O,故答案为:Al2O3+2OH-=2AlO2-+H2O;
(2)若A~E均为化合物.A是淡黄色固体,能发生反应生成B、C,则A是Na2O2,过氧化钠能和水、二氧化碳分别反应生成NaOH、Na2CO3,B、C两溶液在等物质的量浓度时,C 溶液的pH较小,则B是NaOH、C是Na2CO3,电解D的水溶液是最重要的工业生产之一,则D为NaCl,D→E→C也是工业制备C的普遍方法,则E是NaHCO3;
①A是过氧化钠,其电子式为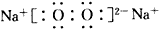 ,故答案为:
,故答案为: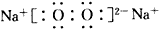 ;
;
②用惰性电极电解氯化钠溶液时,阳极上氯离子放电、阴极上氢离子放电,同时阴极附近生成氢氧根离子,离子方程式为2Cl-+2H2O
H2↑+Cl2↑+2OH-,
故答案为:2Cl-+2H2O
H2↑+Cl2↑+2OH-;
③生铁浸入D溶液而发生吸氧腐蚀,正极上氧气得电子和水生成氢氧根离子,电极反应式为O2+4e-+2H2O=4OH-,故答案为:O2+4e-+2H2O=4OH-;
(3)若A为单质,C、D的相对分子质量相差16,相差一个O原子,0.1mol/L E溶液中只有3种离子,且常温下溶液中的
=1012,溶液呈强酸性,E为酸,符合条件时,A为N2、B为NH3、C为NO、D为NO2、E为HNO3
①B是氨气、C是NO,氨气和氧气在催化剂、加热条件下生成NO和水,反应方程式为4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O;
②A是氮气、C是NO,氮气和氧气的反应中,每转移1mol e-就会吸热45kJ,则转移4mol电子吸收180kJ热量,所以该反应热化学反应方程式为N2(g)+O2(g)=2NO(g)△H=+180 kJ/mol,故答案为:N2(g)+O2(g)=2NO(g)△H=+180 kJ/mol.
(1)若A为单质,B、C均属于盐类,B的水溶液呈酸性,C的水溶液呈碱性,D是一种白色沉淀,A为金属单质,A为Al、B为强酸弱碱盐、C为NaAlO2、D为Al(OH)3、E为Al2O3,
①B为强酸弱碱盐,铝离子水解生成氢氧化铝和氢离子,导致溶液呈酸性,水解方程式为Al3++3H2O?Al(OH)3+3H+,故答案为:Al3++3H2O?Al(OH)3+3H+;
②C是偏铝酸钠,D是氢氧化铝,偏铝酸钠和酸反应生成氢氧化铝沉淀,离子方程式为AlO2-+H++H2O=Al(OH)3↓,故答案为:AlO2-+H++H2O=Al(OH)3↓;
③E是氧化铝、C是偏铝酸钠,氧化铝和氢氧化钠溶液反应生成偏铝酸钠和水,离子方程式为Al2O3+2OH-=2AlO2-+H2O,故答案为:Al2O3+2OH-=2AlO2-+H2O;
(2)若A~E均为化合物.A是淡黄色固体,能发生反应生成B、C,则A是Na2O2,过氧化钠能和水、二氧化碳分别反应生成NaOH、Na2CO3,B、C两溶液在等物质的量浓度时,C 溶液的pH较小,则B是NaOH、C是Na2CO3,电解D的水溶液是最重要的工业生产之一,则D为NaCl,D→E→C也是工业制备C的普遍方法,则E是NaHCO3;
①A是过氧化钠,其电子式为
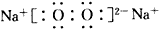 ,故答案为:
,故答案为: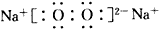 ;
;②用惰性电极电解氯化钠溶液时,阳极上氯离子放电、阴极上氢离子放电,同时阴极附近生成氢氧根离子,离子方程式为2Cl-+2H2O
| ||
故答案为:2Cl-+2H2O
| ||
③生铁浸入D溶液而发生吸氧腐蚀,正极上氧气得电子和水生成氢氧根离子,电极反应式为O2+4e-+2H2O=4OH-,故答案为:O2+4e-+2H2O=4OH-;
(3)若A为单质,C、D的相对分子质量相差16,相差一个O原子,0.1mol/L E溶液中只有3种离子,且常温下溶液中的
| c(H+) |
| c(OH-) |
①B是氨气、C是NO,氨气和氧气在催化剂、加热条件下生成NO和水,反应方程式为4NH3+5O2
| ||
| △ |
| ||
| △ |
②A是氮气、C是NO,氮气和氧气的反应中,每转移1mol e-就会吸热45kJ,则转移4mol电子吸收180kJ热量,所以该反应热化学反应方程式为N2(g)+O2(g)=2NO(g)△H=+180 kJ/mol,故答案为:N2(g)+O2(g)=2NO(g)△H=+180 kJ/mol.
点评:本题以Al、Na、N元素及其化合物为载体考查了无机物推断,根据物质的性质、物质的颜色结合物质之间的转化推断物质,熟悉元素化合物知识并灵活运用这些知识解答问题,题目难度中等.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
下列溶液中的Cl-浓度与50mL 1mol/L MgCl2溶液中的Cl-浓度相等的是( )
| A、150mL 2mol/L KCl溶液 |
| B、75mL 1mol/L CaCl2溶液 |
| C、150mL 1mol/L NaCl溶液 |
| D、75mL 1mol/L AlCl3溶液 |
下列物质中,按照只有氧化性、只有还原性,既有氧化性又有还原性的顺序排列的一组是( )
| A、F2、K、HCl |
| B、Cl2、Al、H2 |
| C、NO2、Na、HNO3 |
| D、O2、SO2、H2O |
在MgCl2和AlCl3的混合液中,Cl-的物质的量为0.7mol.向该溶液中加入100mL 8mol/L的KOH溶液,使之充分反应.若反应前Al3+的物质的量与混合溶液中离子总物质的量的比值为x.以下说法正确的是( )
A、若反应前Al3+的物质的量为a mol,则a=
| ||
| B、只有当x为0.1时,加入87.5mL的KOH,溶液中的阳离子恰好完全沉淀 | ||
| C、当100mL KOH刚好完全消耗,且Al3+全部转化为AlO2-时,x的值为0.2 | ||
| D、x的取值范围是0<x≤0.25 |
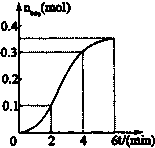 已知CaCO3与稀盐酸的反应为放热反应,取一定量的CaCO3与稀盐酸进行实验,生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )
已知CaCO3与稀盐酸的反应为放热反应,取一定量的CaCO3与稀盐酸进行实验,生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )| A、反应开始后2~4分钟内平均反应速率最大 |
| B、反应刚开始时反应速率较小,然后逐渐增大 |
| C、反应前阶段速率逐渐增大,是因为反应放热,使反应速率加快 |
| D、生成物CaCl2、CO2和H2O的总能量比反应物CaCO3和盐酸的总能量高 |
25℃时,将0.1mol?L-1氨水溶液加水稀释,下列数值变大的是( )
| A、c(OH-) | ||
| B、pH | ||
C、
| ||
| D、c(H+)?c(OH-) |
