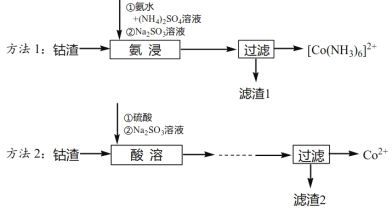
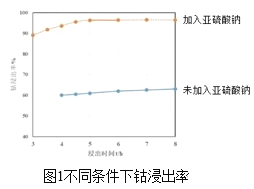
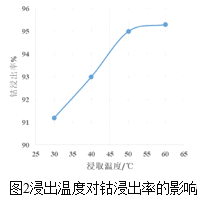
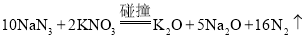��Ŀ����
����Ŀ����2L�ĺ����ܱ������У�ͨ��4mol A��5mol B��������Ӧ��4A(g)��5B(g)��3C(g)��3D(s)��5min��ѹǿ��Ϊԭ����80%����÷�Ӧ��0��5min�ڵ�ƽ����Ӧ���ʿɱ�ʾΪ
A.v(A)��0.24 mol��L��1��min��1B.v(B)��0.15 mol��L��1��min��1
C.v(C)��0.18 mol��L��1��min��1D.v(D)��0.36 mol��L��1��min��1
���𰸡�B
��������
��������ʽ��֪����A��ת����Ϊx����
4A(g)��5B(g)��3C(g)��3D(s)
��ʼʱŨ�ȣ�mol��4 5 0
�ı��Ũ�ȣ�mol��4x 5x 3x
ƽ��ʱŨ�ȣ�mol��4-4x 5-5x 3x
ѹǿ֮�ȵ������ʵ���֮�ȣ���![]() =80%��
=80%��
���x=0.3����÷�Ӧ��0��5min��A����4x=1.2mol��
v(A)= =0.12 mol��L��1��min��1��
=0.12 mol��L��1��min��1��
v(B)=![]() v(A)=0.15mol��L��1��min��1��
v(A)=0.15mol��L��1��min��1��
v(C)=![]() v(A)=0.09mol��L��1��min��1��
v(A)=0.09mol��L��1��min��1��
DΪ���壬Ũ��Ϊ�����������ڱ�ʾ��ѧ��Ӧ���ʡ�
��ѡB��

 ��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д�
��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д� Сѧ��ĩ���Ծ�ϵ�д�
Сѧ��ĩ���Ծ�ϵ�д�����Ŀ�����������Ǵ��������������Ч����֮һ����1L�ĺ����ܱ������г���2mol NH3��1mol NO��1mol NO2��������Ӧ��2NH3(g)��NO(g)��NO2(g)![]() 2N2(g)��3H2O(g)��H���ڲ�ͬ�¶��·���������Ӧ�����N2�����ʵ���(mol)��ʱ��Ĺ�ϵ���±���
2N2(g)��3H2O(g)��H���ڲ�ͬ�¶��·���������Ӧ�����N2�����ʵ���(mol)��ʱ��Ĺ�ϵ���±���
0 | 10 min | 20 min | 30 min | 40 min | |
T1K | 0 | 0.6 | 1.1 | 1.5 | 1.5 |
T2K | 0 | 0.8 | 1.4 | 1.4 | 1.4 |
�ش��������⣺
(1)������Ӧ��___________(����ĸ)��
A. ��S>0����H>0 B. ��S>0����H<0 C. ��S<0����H>0 D. ��S<0����H<0
(2)T1_______(����>����<����������)T2��������___________________________________________
(3)T1K�£�0��20min��v(NO)��______________
(4)T2K�£�NO2��ƽ��ת����Ϊ_____________