题目内容
6.将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示.导致该现象的主要原因是液滴之下氧气含量比边缘少.下列说法正确的是( )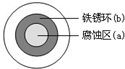
| A. | 液滴中的Cl-由a区向b区迁移 | |
| B. | 液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e-→4OH- | |
| C. | 液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH-形成Fe(OH)2,进一步氧化、脱水形成铁锈 | |
| D. | 若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为:Cu-2e-→Cu2+ |
分析 NaCl溶液滴到一块光亮清洁的铁板表面上,一段时间后在液滴覆盖的圆周中心区(a)被腐蚀变暗,实际上是发生了吸氧腐蚀,这时,负极电极反应为:Fe-2e-=Fe2+ (发生氧化反应)正极电极反应为:O2+2H2O+4e-=4OH- (发生还原反应)在液滴外沿,由于Fe2++2OH-=Fe(OH)2,4Fe(OH)2+O2+2H2O=4Fe(OH)3 形成了棕色铁锈环(b).
解答 解:A.根据在原电池中,阳离子移向正极,阴离子移向负极的规律,Cl-应由b区向a区迁移,故A错误;
B.O2在液滴外沿反应,正极电极反应为:O2+2H2O+4e-=4OH- (发生还原反应),故B正确;
C.液滴下的Fe因发生氧化反应而被腐蚀,故C错误;
D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,由于Fe的金属活动性比铜强,Fe仍为负极,负极发生的电极反应为:Fe-2e-=Fe2+,故D错误.
故选B.
点评 本题考查氧化还原反应、电化学等方面知识,注意在原电池中,阳离子移向正极,阴离子移向负极.

练习册系列答案
相关题目
16.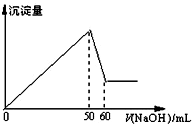 在AlCl3和MgCl2的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中AlCl3与MgCl2的物质的量浓度
在AlCl3和MgCl2的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中AlCl3与MgCl2的物质的量浓度
之比为( )
 在AlCl3和MgCl2的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中AlCl3与MgCl2的物质的量浓度
在AlCl3和MgCl2的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中AlCl3与MgCl2的物质的量浓度之比为( )
| A. | 1:1 | B. | 3:1 | C. | 1:2 | D. | 2:1 |
17.用激光笔照射下列分散系,能观察到丁达尔效应的是( )
| A. | NaCl水溶液 | B. | NaCl与酒精形成的胶体 | ||
| C. | 黄色的FeCl3溶液 | D. | 无色透明的CCl4液体 |
14.下列事实能说明某元素的非金属性比Si强的是( )
| 事实 | 非金属性强弱 | |
| A | CH4受热分解的温度比SiH4高 | C>Si |
| B | C与SiO2在高温下反应生成Si和CO | C>Si |
| C | 稀盐酸与Na2SiO3溶液反应生成H2SiO3胶体 | Cl>Si |
| D | H2SO3是中强酸,H2SiO3是弱酸 | S>Si |
| A. | A | B. | B | C. | C | D. | D |
1.下列水解反应的应用,不正确的是( )
| A. | CO32-+H2O?HCO3-+OH- 热的纯碱溶液清洗油污 | |
| B. | Al3++3H2O?Al(OH)3 (胶体)+3 H+ 明矾净水 | |
| C. | TiCl4+(x+2)H2O(过量)?TiO2•x H2O+4HCl 用TiCl4制备TiO2 | |
| D. | SnCl2+H2O?Sn(OH)Cl+HCl 配制氯化亚锡溶液时应加入氢氧化钠 |
18.乙醇和乙酸是生活中两种常见的有机物.下列说法正确的是( )
| A. | 乙醇、乙酸互为同分异构体 | |
| B. | 乙醇、乙酸都能与钠反应 | |
| C. | 乙醇、乙酸都能与NaOH溶液反应 | |
| D. | 乙醇、乙酸都能使紫色石蕊试液变红色 |
16.NaHCO3在日常生活和工农业生产中有重要用途,关于NaHCO3的说法不正确的是( )
| A. | 是一种钠盐 | B. | 是一种酸式盐 | C. | 水溶液显酸性 | D. | 是一种电解质 |
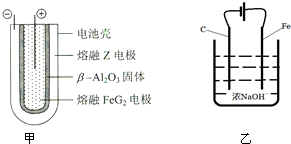 铝、铁是两种重要的金属元素,其单质及化合物在生产生活中的应用日趋广泛.
铝、铁是两种重要的金属元素,其单质及化合物在生产生活中的应用日趋广泛.