题目内容
14.乙酸乙酯与乙醛(CH3CHO)的混合物中氢元素的质量分数为$\frac{1}{11}$,则氧元素的质量分数为( )| A. | $\frac{10}{11}$ | B. | $\frac{4}{25}$ | C. | $\frac{4}{11}$ | D. | $\frac{4}{5}$ |
分析 乙酸乙酯的分子式为C4H8O2,乙醛的分子式为C2H4O,两种物质中C、H原子的数目之比为1:2,故混合物中C、H元素质量之比为12:2=6:1,则根据氢元素的质量分数可计算碳元素的质量分数,进而计算该混合物中氧元素的质量分数.
解答 解:乙酸乙酯的分子式为C4H8O2,乙醛的分子式为C2H4O,两种物质中C、H原子的数目之比为1:2,故混合物中C、H元素质量之比为12:2=6:1,混合物中氢元素的质量分数为$\frac{1}{11}$,则碳元素质量分数为$\frac{1}{11}$×6=$\frac{6}{11}$=,故混合物中氧元素的质量分数为1-$\frac{1}{11}$-$\frac{6}{11}$=$\frac{4}{11}$,故选C.
点评 本题考查元素质量分数的计算,难度不大,关键是根据乙酸乙酯与乙醛的分子式确定C、H原子的质量关系.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
4.下列事实能说明氯元素原子得电子能力比硫元素强的是( )
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强 ③HCl的稳定性比H2S强 ④HCl的还原性比H2S强
⑤HClO的酸性比H2SO4强 ⑥Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑦Cl2能与H2S反应生成S
⑧还原性:Cl->S2-.
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强 ③HCl的稳定性比H2S强 ④HCl的还原性比H2S强
⑤HClO的酸性比H2SO4强 ⑥Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑦Cl2能与H2S反应生成S
⑧还原性:Cl->S2-.
| A. | ③④⑤⑦⑧ | B. | ③⑥⑦ | C. | ③⑥⑦⑧ | D. | ①②③④⑤⑥⑦⑧ |
2.分子式为C3H4Cl2的链状有机物的同分异构体共有(不包括立体异构)( )
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
9.下列说法正确的是( )
| A. | 向海水中加入明矾可以使海水淡化,用于解决淡水供应危机 | |
| B. | 将地沟油回收再加工为食用油,以减缓水体富营养化 | |
| C. | 大力推广农作物的生物防治技术,以减少农药的使用 | |
| D. | 用聚氯乙烯代替木材,生产包装盒、快餐盒等,以减少木材的使用 |
4.化学与生活、社会密切相关.下列说法正确的是( )
| A. | 二氧化硫、二氧化氮和二氧化碳的任意排放都会导致酸雨 | |
| B. | Na2O可用于呼吸面具中作为氧气的来源 | |
| C. | 向煤中加入适量生石灰,可大大减少燃烧产物中SO2的量 | |
| D. | 稀双氧水可作医疗消毒剂,说明H2O2对人体无害 |
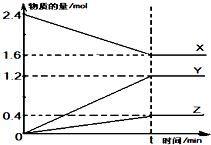 在2L容器中有3种物质进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示,反应在t时刻达到平衡.
在2L容器中有3种物质进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示,反应在t时刻达到平衡.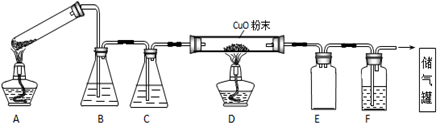

 ;属于共价化合物(填“共价”或“离子”);
;属于共价化合物(填“共价”或“离子”);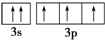 违背了泡利不相容原理;
违背了泡利不相容原理;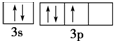 违背了洪特规则.
违背了洪特规则.