题目内容
4.下列事实能说明氯元素原子得电子能力比硫元素强的是( )①HCl的溶解度比H2S大 ②HCl的酸性比H2S强 ③HCl的稳定性比H2S强 ④HCl的还原性比H2S强
⑤HClO的酸性比H2SO4强 ⑥Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑦Cl2能与H2S反应生成S
⑧还原性:Cl->S2-.
| A. | ③④⑤⑦⑧ | B. | ③⑥⑦ | C. | ③⑥⑦⑧ | D. | ①②③④⑤⑥⑦⑧ |
分析 元素的非金属性越强,其原子得电子能力越强,所以可以根据元素的非金属性判断,
利用非金属与氢气化合的难易程度、气态氢化物的稳定性、最高价氧化物的水化物的酸性、非金属单质之间的置换反应等来判断非金属性的强弱,以此来解答.
解答 解:①物质的溶解性属于物理性质,与元素的非金属性及得电子能力无关,所以HCl的溶解度比H2S大,不能说明氯元素原子得电子能力比硫强,故错误;
②不能根据氢化物的水溶液的酸性强弱比较非金属性,例如HI的酸性比HCl强,但非金属性Cl>I;虽硫化氢的酸性比盐酸弱,但非金属性Cl>S,不能说明氯元素原子得电子能力比硫强,故错误;
③元素的非金属性越强,对应氢化物的稳定性越强,氯化氢比硫化氢稳定,可说明氯元素的非金属性比硫元素强,能说明氯元素原子得电子能力比硫强,故正确;
④氯气与H2S能发生置换反应,说明H2S的还原性大于HCl,故错误;
⑤元素的非金属性越强,对应最高价氧化物的水化物的酸性越强,HClO不是最高价氧化物对应的水化物,所以不能比较非金属性,不能说明氯元素原子得电子能力比硫强,故错误;
⑥单质与同种金属反应生成的产物的价态越高,说明氧化性越强,则非金属性越强,所以Cl2与铁反应生成FeCl3,而S与铁反应生成FeS,说明氯气的氧化性大于S,元素的非金属性Cl大于S,能说明氯元素原子得电子能力比硫强,故正确;
⑦元素的非金属性越强,对应单质的氧化性越强,氯气与H2S能发生置换反应,说明氯气的氧化性大于S,元素的非金属性Cl大于S,能说明氯元素原子得电子能力比硫强,故正确;
⑧阴离子的还原性越强,对应元素的非金属性越弱,还原性:Cl-<S2-,故错误;
故选B.
点评 本题考查元素原子得电子能力的比较,可以从非金属性的角度判断,题目难度不大,注意非金属性的递变规律以及比较非金属性的角度.

 同步练习强化拓展系列答案
同步练习强化拓展系列答案
| A. | 对粗盐溶液除杂可依次加入NaOH、Na2CO3、BaCl2,再加入盐酸调节溶液pH | |
| B. | 饱和食盐水中先通入的气体为CO2 | |
| C. | 流程图中的系列操作中一定需要玻璃棒 | |
| D. |  如图所示装置可以比较Na2CO3和NaHCO3晶体的热稳定性 |
| A. | 离子半径:D+>C- | |
| B. | EA2是原子晶体 | |
| C. | A和B形成的原子个数比为1:1的化合物分子是非极性分子 | |
| D. | 以上元素中形成的最高价氧化物对应的水化物酸性最强的是C |
| A. | 容器的总压强不随时间而变化 | |
| B. | 容器内气体的密度不再改变 | |
| C. | 单位时间内有nmolA2生成的同时有nmolB2消耗 | |
| D. | v正(A2)=2v逆(AB) |
| A. | HCl的溶解性强于H2S | B. | 氯的最高价为+7价 | ||
| C. | HCl的稳定性强于H2S | D. | HClO的氧化性强于H2SO4 |
| A. | 500℃时比室温更有利于合成氨的反应 | |
| B. | 红棕色的NO2加压后颜色先变深后变浅 | |
| C. | SO2催化氧化成SO3的反应,往往加入过量的空气 | |
| D. | 实验室中常用排饱和食盐水的方法收集氯气 |
| A. | $\frac{10}{11}$ | B. | $\frac{4}{25}$ | C. | $\frac{4}{11}$ | D. | $\frac{4}{5}$ |
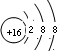 .X与Y形成的离子化合物的电子式为
.X与Y形成的离子化合物的电子式为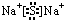 ,Z和Y的最高价氧化物对应的水化物反应的离子方程式为H++OH-=H2O.
,Z和Y的最高价氧化物对应的水化物反应的离子方程式为H++OH-=H2O.