题目内容
4.化学与生活、社会密切相关.下列说法正确的是( )| A. | 二氧化硫、二氧化氮和二氧化碳的任意排放都会导致酸雨 | |
| B. | Na2O可用于呼吸面具中作为氧气的来源 | |
| C. | 向煤中加入适量生石灰,可大大减少燃烧产物中SO2的量 | |
| D. | 稀双氧水可作医疗消毒剂,说明H2O2对人体无害 |
分析 A、二氧化碳能参与生态环境的循环;
B、Na2O无论是与水还是与CO2反应均不能生成氧气;
C、生石灰CaO是碱性氧化物,能和酸性氧化物反应生成盐;
D、H2O2有较强的氧化性,能引起蛋白质的变性.
解答 解:A、二氧化碳能参与生态环境的循环,不是大气污染物,不能引起酸雨,故A错误;
B、Na2O无论是与水还是与CO2反应均不能生成氧气,不能作为氧气的来源,能作为氧气来源的是过氧化钠,故B错误;
C、生石灰CaO是碱性氧化物,能和酸性氧化物反应生成盐,故生石灰能吸收燃烧产物中的SO2,减少对空气的污染,故C正确;
D、H2O2有较强的氧化性,能引起蛋白质的变性,故过量的使用也对人体有害,故D错误.
故选C.
点评 本题主要考查了过氧化氢的性质、做供氧剂的物质以及碱性氧化物的性质,属于基础性知识,题目难度不大.

练习册系列答案
相关题目
14.乙酸乙酯与乙醛(CH3CHO)的混合物中氢元素的质量分数为$\frac{1}{11}$,则氧元素的质量分数为( )
| A. | $\frac{10}{11}$ | B. | $\frac{4}{25}$ | C. | $\frac{4}{11}$ | D. | $\frac{4}{5}$ |
15.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1mol甲基中含电子数目为7NA | |
| B. | 标准状况下,22.4L己烷中共价键数目为19NA | |
| C. | 14g乙烯和丁烯的混合物中含有的原子总数为3NA个 | |
| D. | 1mol苯乙烯(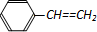 )中含有的C=C数为4NA )中含有的C=C数为4NA |
19.用括号内试剂及操作方法除去下列各物质中的少量杂质,不正确的是( )
| A. | 乙醇中的水(CaO、蒸馏) | B. | 溴乙烷中的乙醇(水、分液) | ||
| C. | 苯中的甲苯(Br2水、分液) | D. | 溴苯中的溴(NaOH溶液、分液) |
9.下列有关阿佛加德罗常数(NA)的说法正确的有( )
| A. | 标准状况下,22.4L SO3所含的分子数目为NA | |
| B. | 0.2molH2O2催化分解,转移电子数为0.2NA | |
| C. | 0.1mol/L的100mLH2SO3溶液中,含有的离子数约为0.03NA | |
| D. | 6.25 mL1 mol/L浓硫酸与足量铜反应,转移电子数为0.2NA |
16.元素周期表的一部分,按要求完成各小题.(9分)
(1)化学性质最不活泼的元素Ar,非金属性最强的元素是F.(填元素符号)
(2)金属性最强的单质与水反应的化学方程式为:2K+2H2O═2KOH+H2↑①③⑤三种元素的最高价氧化物水化物中,碱性最强的NaOH(写化学式).
(3)某元素的最高价氧化物的水化物既能与强酸反应生成盐A和水又能与强碱反应生成盐B与水,写出盐B溶液与小苏打溶液反应的离子方程式AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-,向该元素和⑧号元素组成的化合物溶液中,缓缓滴加NaOH至过量,现象为:随着氢氧化钠的滴入,白色沉淀逐渐增加,当达到最多后又逐渐减少,最后完全消失,得到澄清溶液.
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ⑥ | ⑦ | ⑨ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑪ |
(2)金属性最强的单质与水反应的化学方程式为:2K+2H2O═2KOH+H2↑①③⑤三种元素的最高价氧化物水化物中,碱性最强的NaOH(写化学式).
(3)某元素的最高价氧化物的水化物既能与强酸反应生成盐A和水又能与强碱反应生成盐B与水,写出盐B溶液与小苏打溶液反应的离子方程式AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-,向该元素和⑧号元素组成的化合物溶液中,缓缓滴加NaOH至过量,现象为:随着氢氧化钠的滴入,白色沉淀逐渐增加,当达到最多后又逐渐减少,最后完全消失,得到澄清溶液.
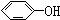 与
与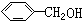
 与
与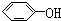
 现用邻苯二甲酸氢钾(本题中用KHA表示)标准溶液来测定某NaOH溶液的浓度,进行如下操作:
现用邻苯二甲酸氢钾(本题中用KHA表示)标准溶液来测定某NaOH溶液的浓度,进行如下操作: